引言
外泌体是细胞间信息传递的核心膜囊泡载体,在肿瘤进展、免疫调控与病毒感染中至关重要,但其释放调控机制长期未被系统阐明。中国科学院上海药物研究所钟劲团队新研究揭示,己糖胺生物合成通路(HBP)可通过介导SNAP25蛋白O-GlcNAc糖基化,增强SNARE复合体装配效率,驱动多泡体与质膜融合,进而调控外泌体释放。该发现首次建立糖代谢旁路与外泌体分泌的直接分子关联,为解析肿瘤高代谢—高外泌体表型提供关键理论支撑,也为肿瘤干预提供全新代谢靶点。

一、糖代谢对外泌体释放的普遍性调控
研究团队首先证实糖代谢水平直接决定外泌体分泌效率,且具有广谱性:
1. 以半乳糖替代葡萄糖培养肝癌Huh7、胚胎肾HEK293T、肺腺癌A549等细胞,糖酵解显著受抑,外泌体释放量大幅下降;
2. 降低葡萄糖浓度或用2-脱氧葡萄糖(2-DG)抑制糖酵解,可重复上述表型;
3. 细胞内MVB形成与内涵体内泡(ILV)数量无明显减少,但MVB在核周聚集、运动能力下降,提示调控发生在MVB运输与膜融合环节,而非早期生成阶段。
上述结果证明,糖代谢并非仅影响外泌体生物合成,而是精准控制其胞内运输与胞外释放的关键上游信号。
二、HBP通路与O-GlcNAc修饰的核心调控作用
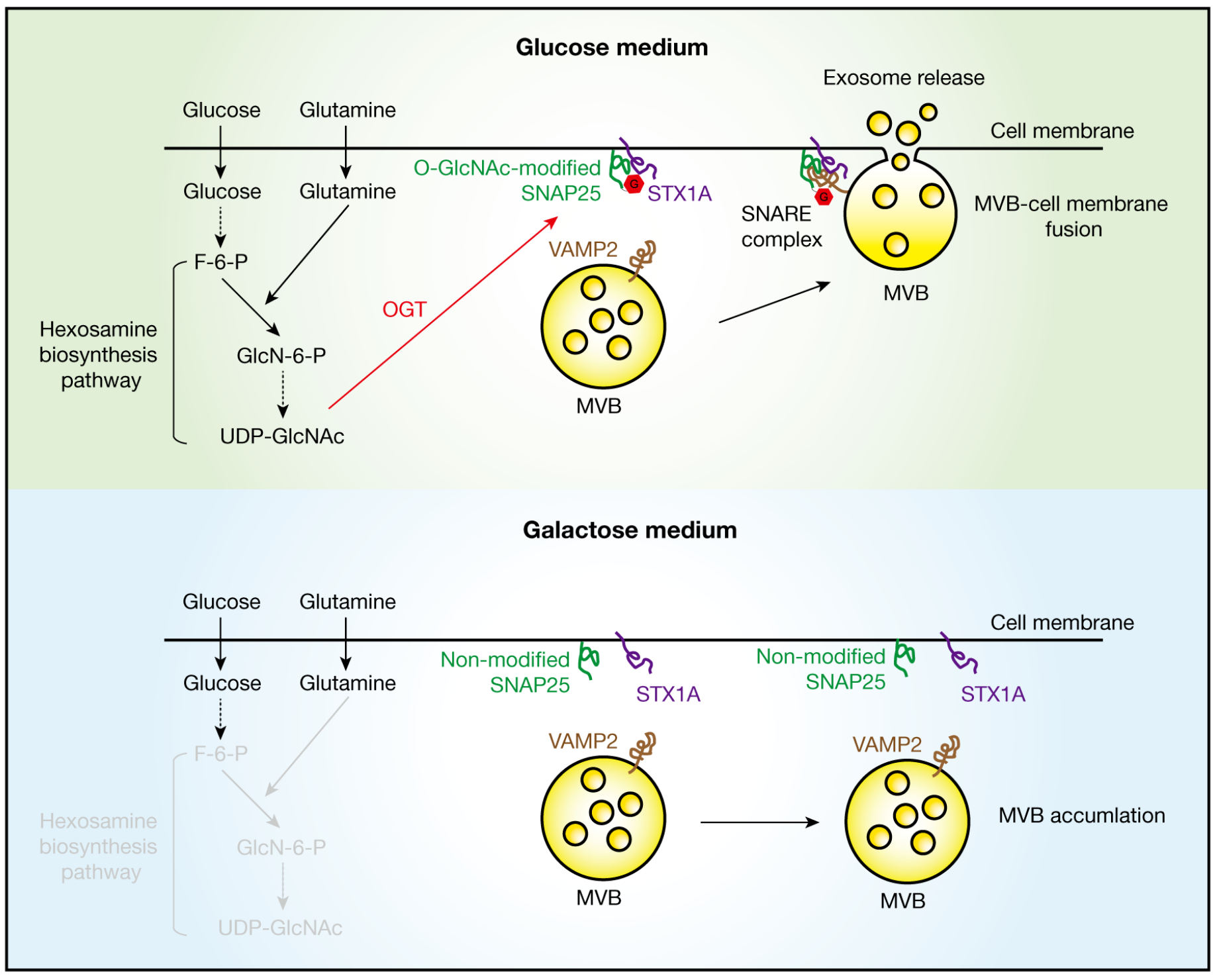
HBP通过调节SNAP25的O-GlcNAcylation调控外泌体释放
HBP是连接糖代谢与蛋白翻译后修饰的关键旁路,其限速酶为GFPT1,终产物UDP-GlcNAc由OGT催化完成蛋白O-GlcNAc修饰。团队通过功能实验明确HBP-O-GlcNAc轴的必要性与充分性:
1. 敲低GFPT1、抑制OGT活性或剥夺谷氨酰胺,均降低整体O-GlcNAc水平并抑制外泌体释放;
2. 提升细胞O-GlcNAc水平,可部分恢复外泌体分泌能力;
3. 该通路不改变MVB数量,仅影响其向质膜转运与融合,与前期表型一致。 该结果首次确立HBP及O-GlcNAc修饰是外泌体释放的必需代谢环节,将糖代谢流与囊泡分泌直接耦联。
三、分子机制:SNAP25糖基化驱动SNARE复合体装配
SNARE复合体是囊泡与靶膜融合的核心分子机器,由SNAP25、STX1A、VAMP2等组成。团队进一步锁定关键效应分子:
1. 葡萄糖浓度升高可特异性增强SNAP25的O-GlcNAc修饰水平;
2. SNAP25高糖基化显著促进其与STX1A、VAMP2的相互作用,提升SNARE复合体装配效率;
3. 高效装配的SNARE复合体加速MVB与质膜融合,最终促进外泌体释放。
由此完整阐明分子通路:葡萄糖→HBP激活→UDP-GlcNAc升高→SNAP25 O-GlcNAc修饰增强→SNARE装配加速→MVB-质膜融合→外泌体释放上调。
四、研究意义与转化前景
(一)科学意义
1. 建立代谢-修饰-囊泡分泌的全新调控轴,系统解释肿瘤高代谢伴随高外泌体分泌的分子基础;
2. 拓展O-GlcNAc修饰的生理功能,首次证实其调控囊泡膜融合机器,丰富糖基化修饰的调控图谱;
3. 明确外泌体释放调控的代谢检查点,为细胞通讯与肿瘤微环境研究提供新维度。
(二)临床转化潜力
1. 靶点开发:HBP通路(GFPT1、OGT)与SNAP25糖基化位点可作为外泌体抑制剂的筛选靶点,用于阻断肿瘤信号传递;
2. 疾病标志物:外周血O-GlcNAc水平与外泌体含量可联合作为肿瘤代谢异常的无创监测指标;
3. 干预策略:靶向HBP-SNAP25轴,既可抑制肿瘤外泌体介导的侵袭转移,也可调控免疫微环境,具备联合治疗潜力。
五、总结与展望
钟劲团队的研究突破性揭示己糖胺生物合成通路通过O-GlcNAc修饰SNAP25调控外泌体释放,完成从代谢通路到分子效应的全链条解析,为代谢调控囊泡分泌领域树立新范式。 未来研究可聚焦:
① HBP轴在不同肿瘤亚型中的特异性调控差异;
② O-GlcNAc修饰SNAP25的精确位点与结构基础;
③ 靶向该轴的小分子抑制剂研发与体内验证。随着机制深化与技术突破,靶向糖代谢 外泌体调控轴有望成为肿瘤精准治疗的新方向。