近日,国际顶刊《Nature》发表一项突破性研究:研究团队成功构建CD8⁺T细胞综合性转录因子调控图谱,系统揭示了T细胞不同分化状态的核心调控机制,首次精准识别出可选择性调控T细胞衰竭程序的关键因子。

一、研究核心背景:两种“形似神异”的T细胞
研究聚焦CD8⁺T细胞中两类关键细胞状态:
终末耗竭T细胞(TEXterm):功能障碍型,抑制抗肿瘤免疫
组织驻留记忆T细胞(TRM):保护型,强效抑制肿瘤 二者转录水平高度相似,但功能完全相反,是T细胞免疫治疗的核心调控靶点。
二、多组学解析:绘制T细胞分化调控全景图
研究团队整合121个CD8⁺T细胞样本的转录组与染色质可及性数据,覆盖9种T细胞状态,构建完整基因调控网络,系统计算转录因子活性。
核心发现:
1. 共鉴定309个关键转录因子,含136个单状态因子、173个多状态因子;
2. 锁定34个TEXterm特异性因子、20个TRM特异性因子;
3. 证实TEXterm与TRM受完全不同的转录因子网络调控,为精准干预提供依据;
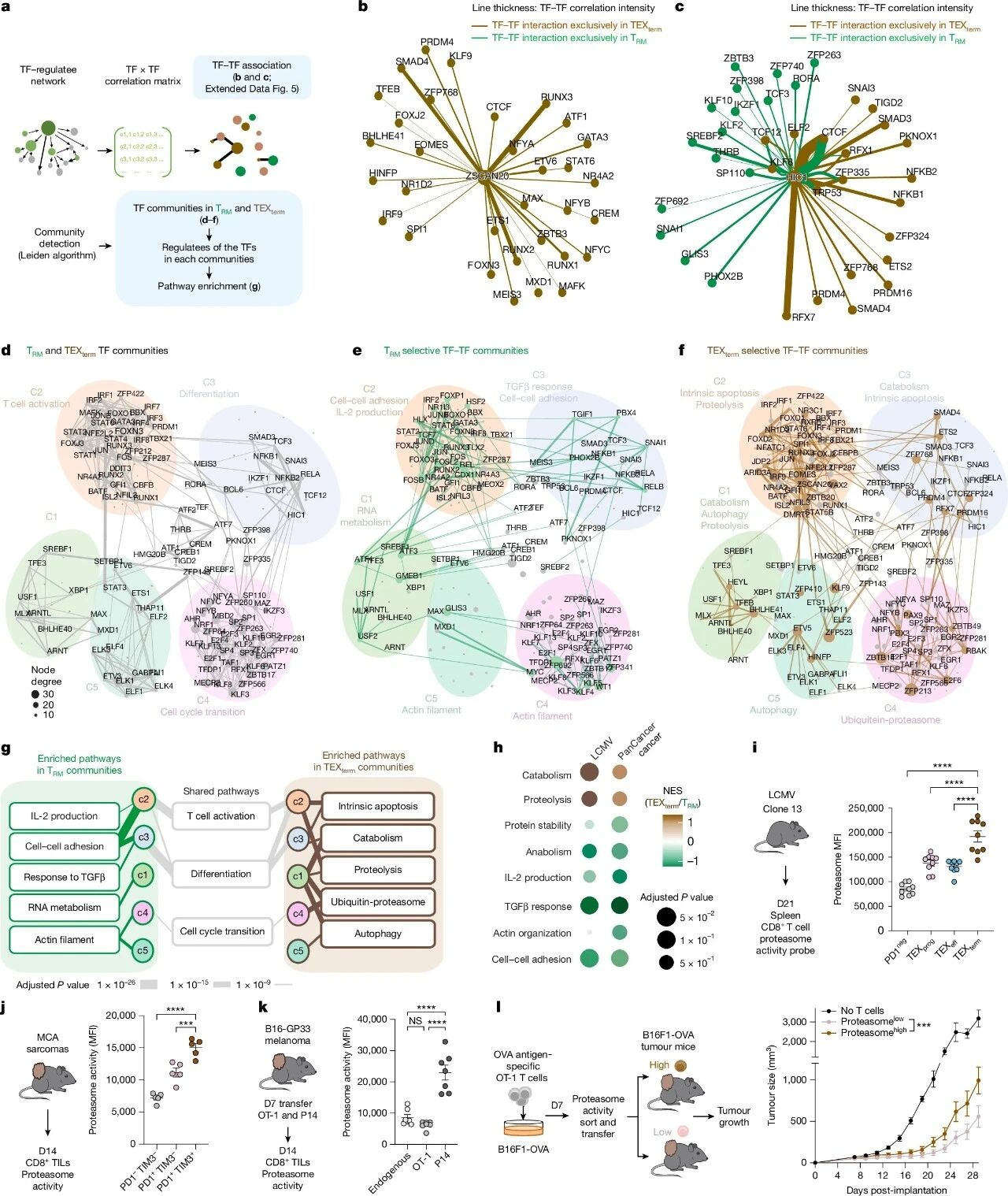
TEXterm与TRM细胞状态中转录因子网络的全局分析
三、创新筛选平台:体内Perturb-seq鉴定关键靶点
团队搭建体内CRISPR筛选+单细胞RNA测序的Perturb-seq平台,在慢性感染模型中对19个候选转录因子进行功能验证。
突破性新因子:
ZSCAN20:敲除可降低TEXterm分化54%,增强T细胞效应功能
JDP2:敲除可降低TEXterm分化43%,提升免疫活性
上述两个因子为全新发现,此前无T细胞功能相关报道。
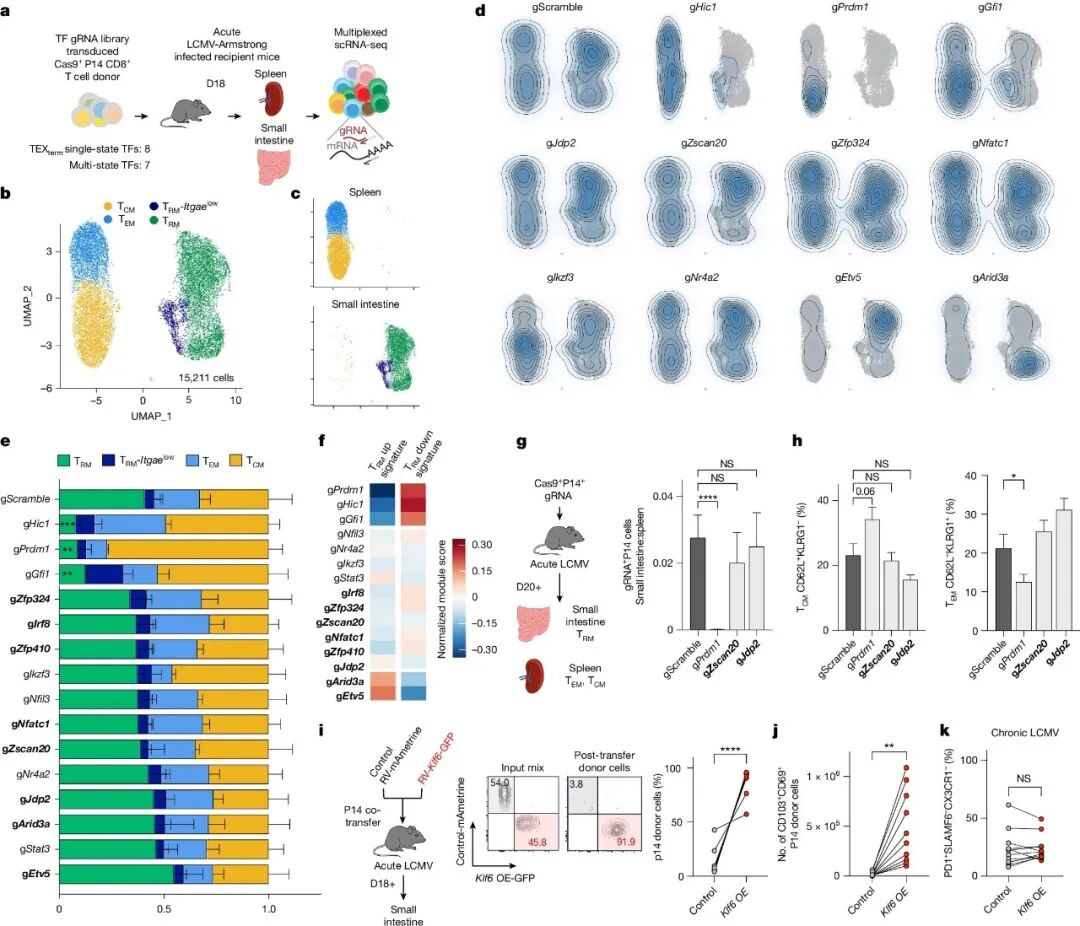
在TEXterm与TRM分化中具有不同作用的转录因子的功能验证
四、精准编程:定向引导T细胞走向“保护型”
本研究最具临床价值的结论:
1. 靶向TEXterm特异性转录因子,不影响TRM细胞生成;
2. 可将T细胞精准导向保护性TRM状态,避免耗竭;
3. KLF6为TRM特异性因子,过表达可促进TRM形成,不加剧耗竭 该技术实现T细胞状态精准定向编程,突破传统免疫治疗“误伤有益细胞”的瓶颈。
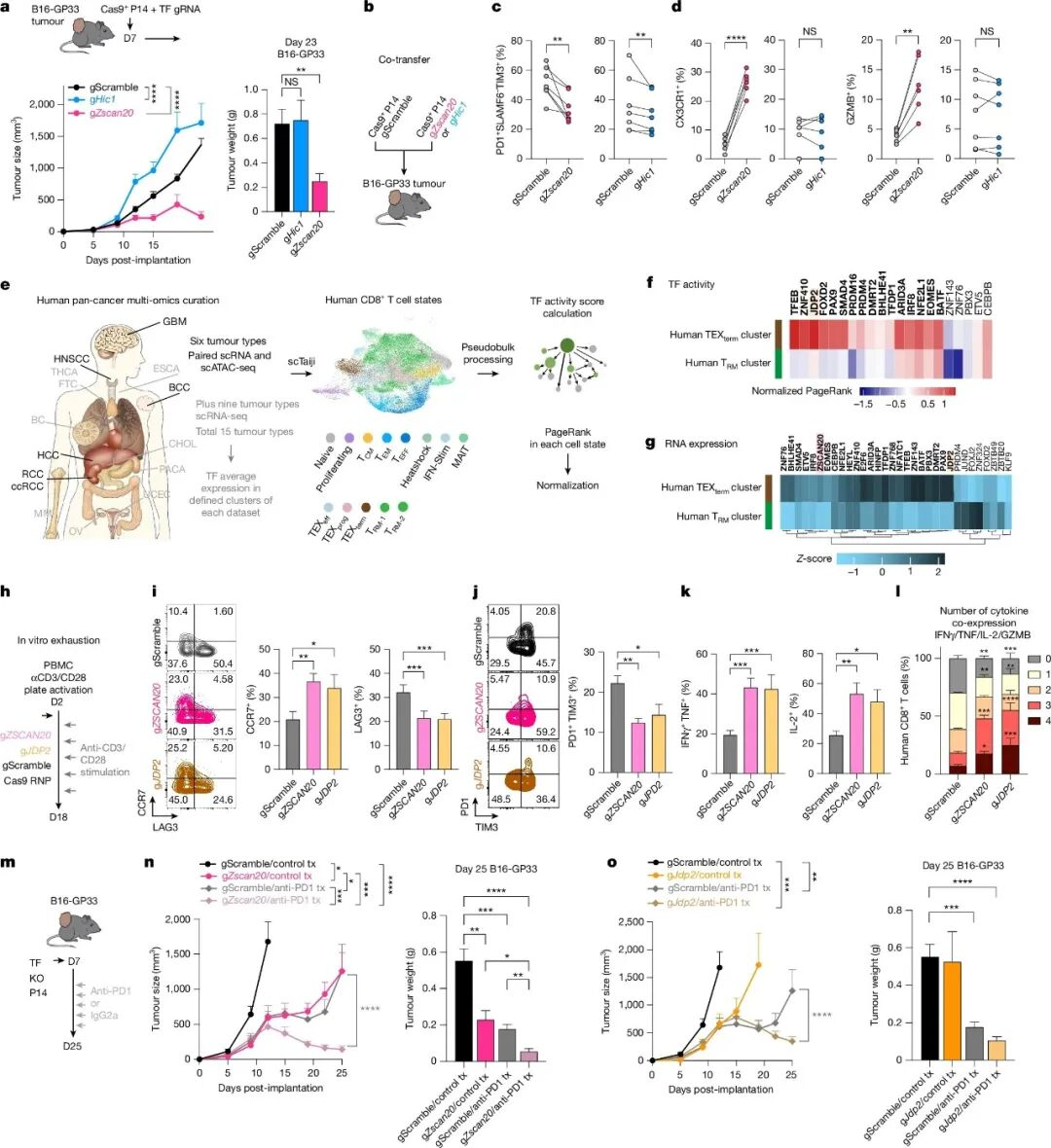
靶向TEXterm单状态转录因子可增强肿瘤控制
五、跨物种验证:人类肿瘤中同样适用
研究分析人类肿瘤浸润CD8⁺T细胞数据证实:
1. 小鼠中鉴定的TEXterm相关转录因子,在人类T细胞中同样富集激活;
2. 敲除ZSCAN20/JDP2可降低人T细胞抑制受体表达、提升效应因子分泌;
3. ZSCAN20/JDP2敲除+抗PD-1治疗,呈现显著协同抗肿瘤效果。
六、研究意义与临床价值
1. 首次完整绘制CD8⁺T细胞分化转录因子图谱;
2. 发现全新T细胞耗竭调控靶点ZSCAN20、JDP2;
3. 建立不损伤保护性TRM的精准调控策略;
4. 为新一代CAR-T、TCR-T等细胞治疗提供核心靶点;
5. 为免疫检查点抑制剂提供高效联合治疗方案。