一、肿瘤免疫微环境的细胞与分子调控特征
肿瘤被视为一个复杂的生态系统,其中癌细胞与宿主细胞之间的相互作用深刻影响疾病进展及治疗响应。在众多宿主细胞中,免疫细胞尤其是实体瘤中最具异质性的组分,其功能可从抗肿瘤延伸至促肿瘤方向。在肿瘤演进过程中,癌细胞通过多种机制逃避免疫识别与攻击,例如下调抗原呈递相关分子或诱导抑制性免疫检查点分子的表达。与此同时,癌细胞还可劫持中性粒细胞、巨噬细胞及调节性T细胞(Treg细胞)等免疫细胞,从而构建免疫抑制性的肿瘤微环境。这一微环境不仅促进了免疫逃逸,还推动了脉管系统与细胞外基质的重塑,进而支持肿瘤的持续进展及治疗抵抗。因此,异常免疫反应已被视为癌症的核心特征之一,并为癌症治疗提供了关键靶点,免疫检查点阻断疗法的成功即为典型例证。
近年来,用于解析肿瘤细胞空间构型及单个细胞分子特征的技术取得了长足发展。特别是单细胞分析与空间转录组分析等技术,为揭示肿瘤微环境的异质性提供了新的视角。同时,这些技术也揭示了不同癌症类型内部特征及其免疫景观之间的显著差异。本文重点聚焦于遗传变异、表观遗传修饰、细胞信号通路及代谢改变等癌细胞固有特征,这些因素在塑造癌症免疫景观中发挥关键作用。
二、遗传异常与肿瘤免疫
癌症基因组中常发生多种体细胞改变,包括点突变、DNA片段插入或缺失、基因扩增及重排等。其中部分改变作为“驱动事件”参与肿瘤的发生与进展,而另一些作为“伴随事件”对癌细胞生长无直接影响。近年来,通过将高通量测序技术与高分辨率免疫图谱相结合,研究者对人类肿瘤进行了系统分析,以揭示遗传畸变与免疫表型之间的关联,免疫肿瘤学领域因此获得了重要进展。这些研究还发现了多个新的肿瘤基因与免疫表型之间的相关性。本部分重点关注那些影响肿瘤免疫结构及免疫治疗反应的特定癌基因、抑癌基因及DNA损伤修复机制。这些遗传畸变能够重塑免疫微环境格局,并调控肿瘤对免疫治疗的响应。已有临床证据证实了上述遗传因素的免疫调节作用(图1)。
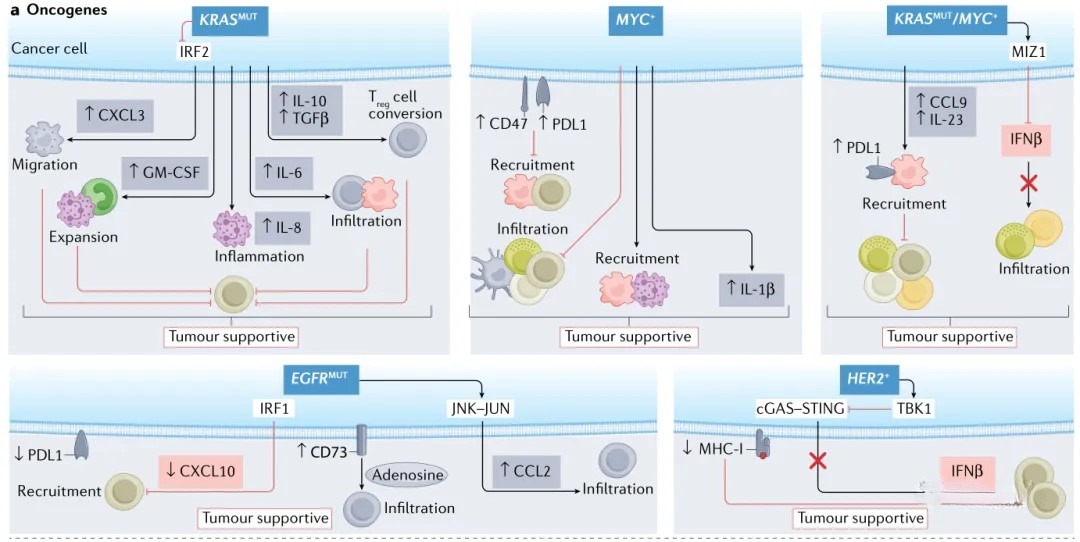
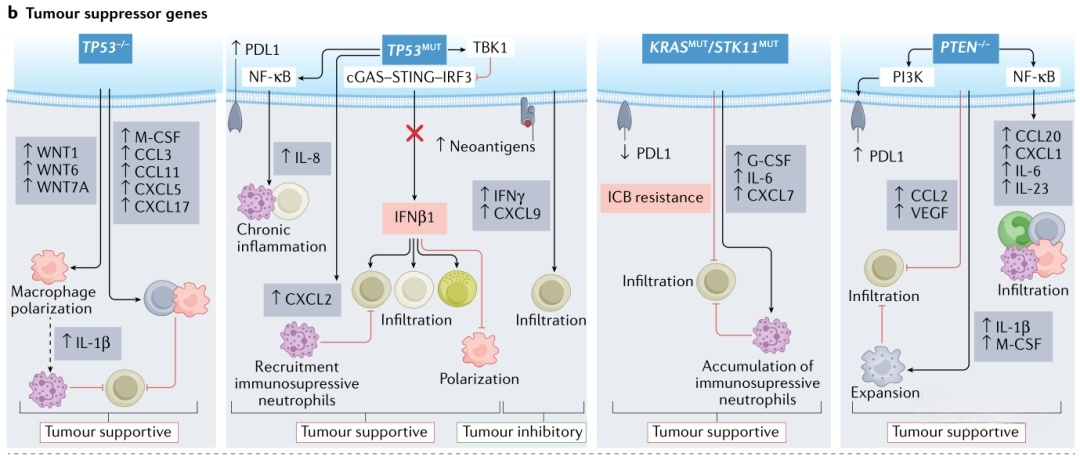
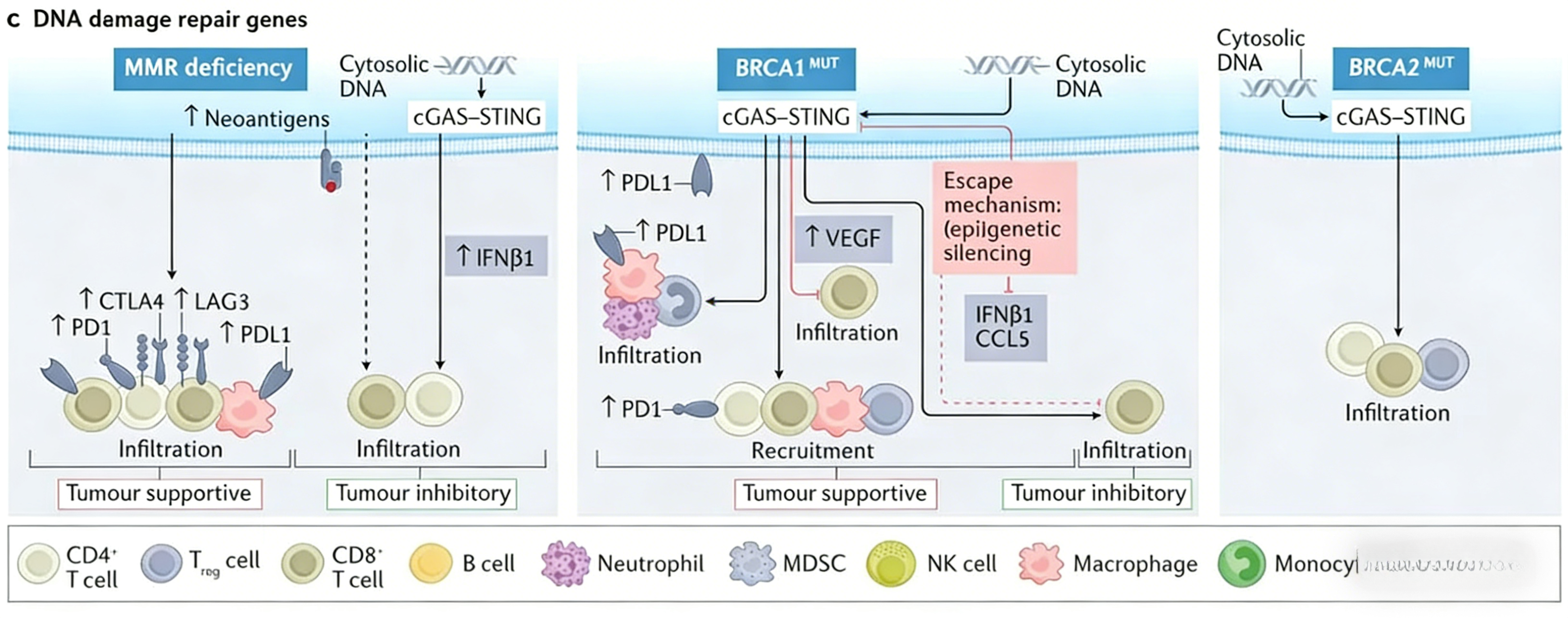 图1 癌症基因分型与免疫表型的关系
图1 癌症基因分型与免疫表型的关系
MYC是人类肿瘤中最常见的激活型癌蛋白之一,也是目前研究最为深入的癌基因。事实上,在绝大多数癌症中均可观察到MYC突变或其相关通路的表达上调。MYC蛋白作为细胞程序的核心调控因子,其激活状态下的癌细胞表现出持续增殖及无限复制的生物学特征。有研究显示,MYC表达水平与人类三阴乳腺癌中免疫信号的丧失之间存在强相关性。在三阴乳腺癌小鼠模型中,MYC的过度表达显著减少了肿瘤内的淋巴细胞浸润,并重塑了免疫信号。进一步在人类三阴乳腺癌细胞系中的研究证实,MYC能够介导抑制性炎症信号的传导。综上所述,已有数据表明MYC可抑制先天免疫并促进肿瘤免疫逃逸,这解释了为何MYC高表达的三阴乳腺癌具有较差的免疫原性。
三、表观遗传修饰与肿瘤免疫
除遗传改变外,表观遗传修饰亦是癌细胞的重要特征之一,在核结构维持与基因转录调控中发挥关键作用。表观遗传改变主要表现为在不改变DNA序列的前提下,导致基因表达与细胞表型发生变化。癌症表观基因组可经历多种类型的改变,包括DNA甲基化、组蛋白修饰、染色质重塑及非编码RNA表达失调。越来越多的证据表明,肿瘤中的表观遗传变化同样能够影响免疫系统(图2)。表观遗传修饰可塑造肿瘤免疫景观,因此,解析癌症表观基因组如何调控免疫行为,将成为未来研究的重要方向。
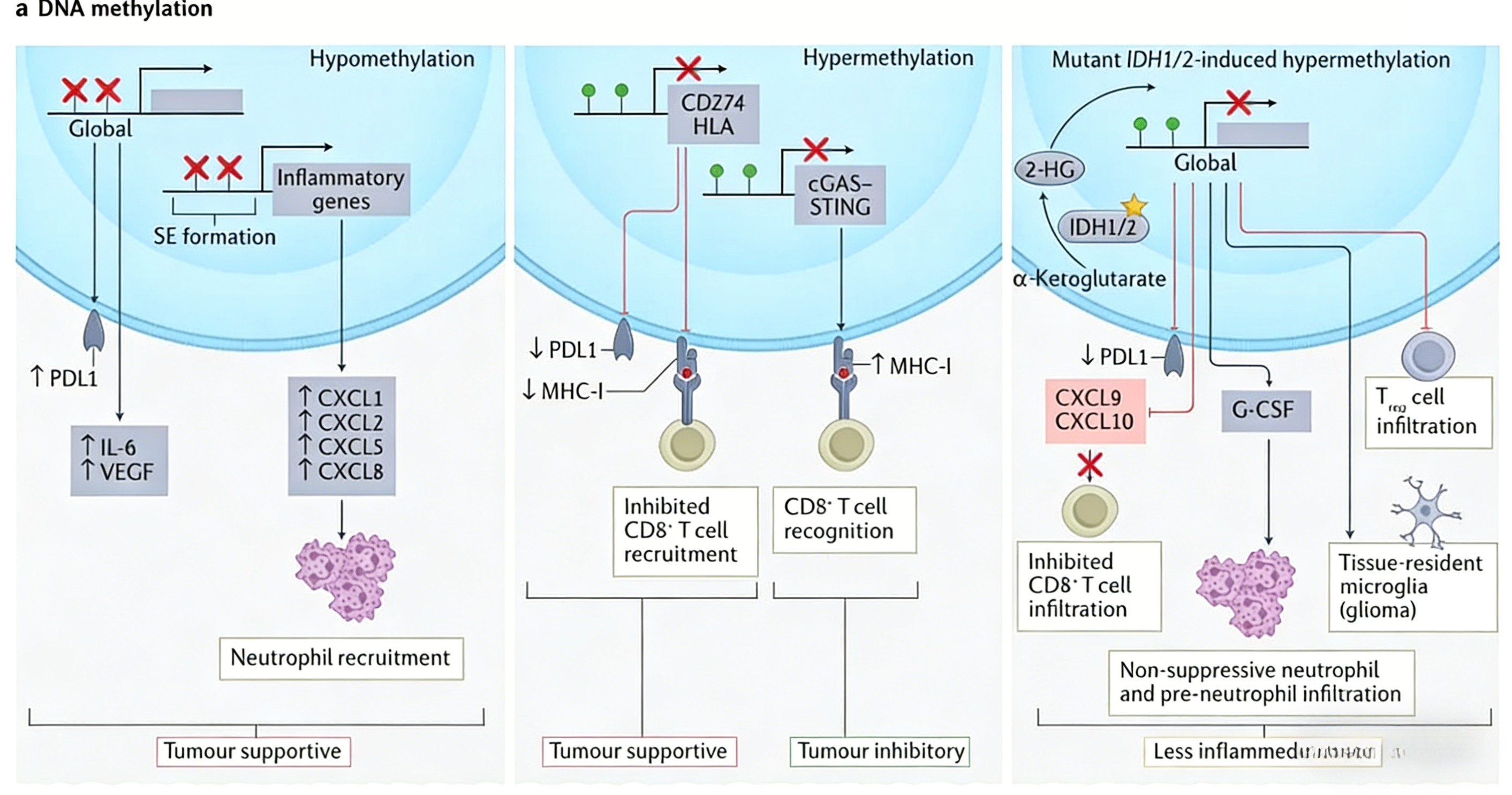
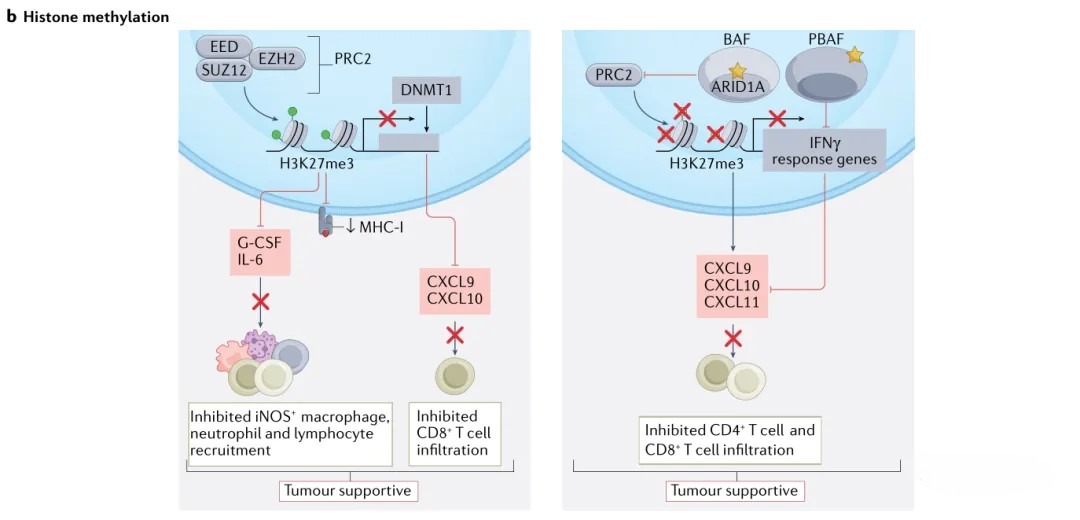
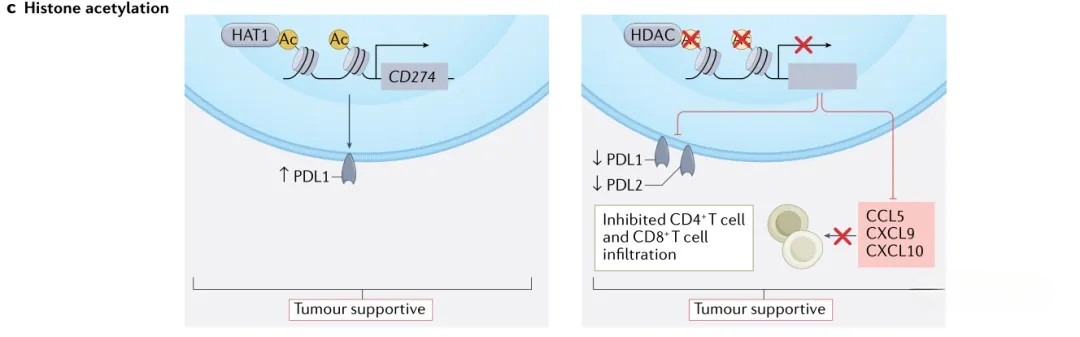 图2 DNA甲基化、组蛋白修饰影响肿瘤免疫景观
图2 DNA甲基化、组蛋白修饰影响肿瘤免疫景观
甲基化是蛋白质与核酸的一种重要修饰方式,能够调控基因的表达与沉默,并与癌症、衰老、阿尔茨海默病等多种疾病密切相关,是表观遗传学的重要研究内容之一。最常见的甲基化修饰形式包括DNA甲基化与组蛋白甲基化。DNA甲基化是DNA化学修饰的一种形式,可在不改变DNA序列的前提下,影响遗传表现。在淋巴细胞的激活与增殖过程中,部分甲基化区域会发生低甲基化。在这些区域中,CpG位点的甲基化状态可用于区分不同免疫细胞(例如通过solo-WCGW模式进行预测)。在一项研究中,作者旨在分析免疫细胞与结肠上皮细胞的全基因组DNA甲基化图谱,以识别CD8⁺T细胞中差异甲基化位点。随后,基于这些差异甲基化位点构建了CD8⁺MeTIL评估体系,用于分析CD8⁺肿瘤浸润淋巴细胞与癌症生存结局之间的关系。最终,相关实验验证了该评估体系的有效性。
四、代谢与肿瘤免疫
在肿瘤发生与发展过程中,癌细胞及其所处的肿瘤微环境常暴露于恶劣条件与多种应激之下。为维持生存与生长,细胞必须适应环境变化。细胞代谢重编程是指细胞为满足能量需求,通过改变代谢模式以促进增殖与生长的机制。该过程不仅有助于细胞抵御外界胁迫,还可能赋予细胞新的功能。癌症代谢与免疫抑制及免疫逃逸密切相关。然而,调控癌细胞与免疫细胞代谢重编程的信号通路与机制仍难以阐明。细胞内在机制与细胞外营养竞争均与代谢改变相关,但不同细胞之间代谢物的相互作用尚不明确。由于代谢组学处于基因组与蛋白质组的下游,能够补充二者信息,因而更贴近生物体的表型。在医学研究中,代谢组学主要应用于疾病诊断、代谢谱分析、药物靶点筛选、预后评估及个体化治疗等领域,已成为后基因组时代的研究热点(图3)。
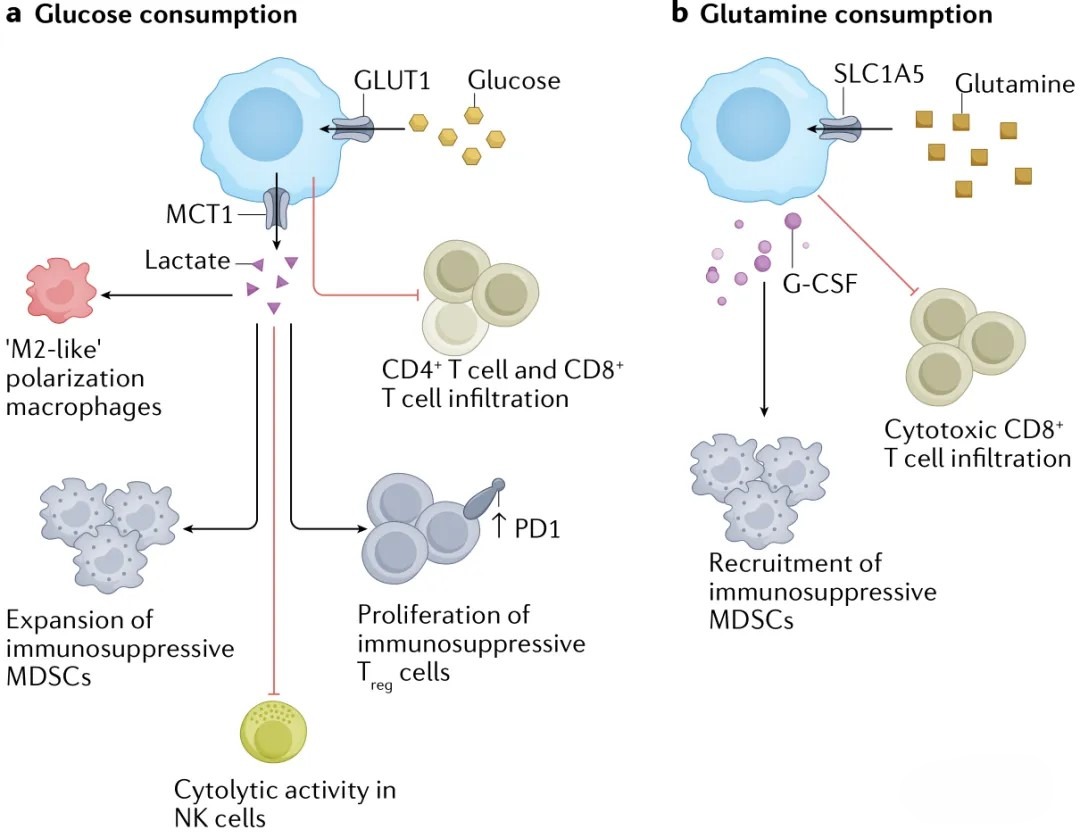 图3 癌细胞的代谢重新编程会影响免疫行为
图3 癌细胞的代谢重新编程会影响免疫行为
肿瘤微环境包含多种细胞类型,每种细胞均处于特定微环境中。因此,在单细胞分辨率下研究代谢异质性具有重要意义。有研究在单细胞水平上分析了肿瘤细胞内的代谢基因表达谱、肿瘤细胞与相邻细胞的代谢通路活性、各类细胞中代谢基因表达的异质性,以及特定细胞类型的代谢重编程[4]。通过对代谢基因表达谱进行聚类分析,发现肿瘤细胞的代谢基因具有高度可塑性,不同患者来源的肿瘤细胞表现出各异的代谢表达谱特征。利用已发表的黑色素瘤与头颈部鳞状细胞癌单细胞数据,该研究进一步分析了不同免疫细胞亚型之间的代谢特征。例如,T细胞可分化为CD8⁺与CD4⁺亚型,其中CD4⁺T细胞可进一步分为调节性T细胞与辅助性T细胞。结果显示,CD4⁺T细胞中氧化磷酸化通路的表达活性显著高于CD8⁺T细胞;而调节性T细胞中的糖酵解途径与氧化磷酸化通路的表达活性均显著高于辅助性T细胞。这些结果表明,免疫细胞的分化过程伴随代谢重编程,导致不同亚型细胞具有各自独特的代谢特征。
五、免疫系统与肿瘤的相互作用
肿瘤细胞作为一种异常分化的细胞,具有持续增殖并偏离正常功能的能力。在生理状态下,免疫系统能够识别并清除缺陷、死亡或凋亡的细胞,主要负责抵御外来入侵者及清除变异细胞。在肿瘤发生初期,癌细胞试图通过各种机制逃避和欺骗免疫细胞,以防止被清除。它们模仿正常细胞的行为,并分泌转化生长因子β等因子,干扰免疫细胞的识别与检查功能。随着肿瘤负荷的不断增加,癌细胞开始主动攻击免疫系统。它们通过释放多种因子破坏免疫细胞的功能,同时影响机体多个生理系统,如损害骨髓与淋巴组织产生免疫细胞的能力,从而削弱免疫功能。这一过程最终可导致免疫系统的全面崩溃。
免疫系统与肿瘤之间的关系已成为当前癌症研究的重要课题之一。过去,人们普遍认为癌症仅由肿瘤本身引起;然而,当前研究已明确,肿瘤的发生与发展依赖于多种细胞和细胞因子的协同支持,即肿瘤微环境。在肿瘤微环境的各类组成成分中,免疫细胞在支持肿瘤方面发挥关键作用。尽管在正常的癌症免疫监视过程中,免疫细胞能够识别并清除新生肿瘤细胞,但在癌症免疫编辑过程中,它们可能受到肿瘤存在所引发的多种因素影响。免疫细胞既可发挥保护作用(即抗肿瘤免疫),也可作为肿瘤的旁观者或支持者(即促肿瘤免疫),这一双重功能使其成为肿瘤微环境中的一把“双刃剑”(图4)。
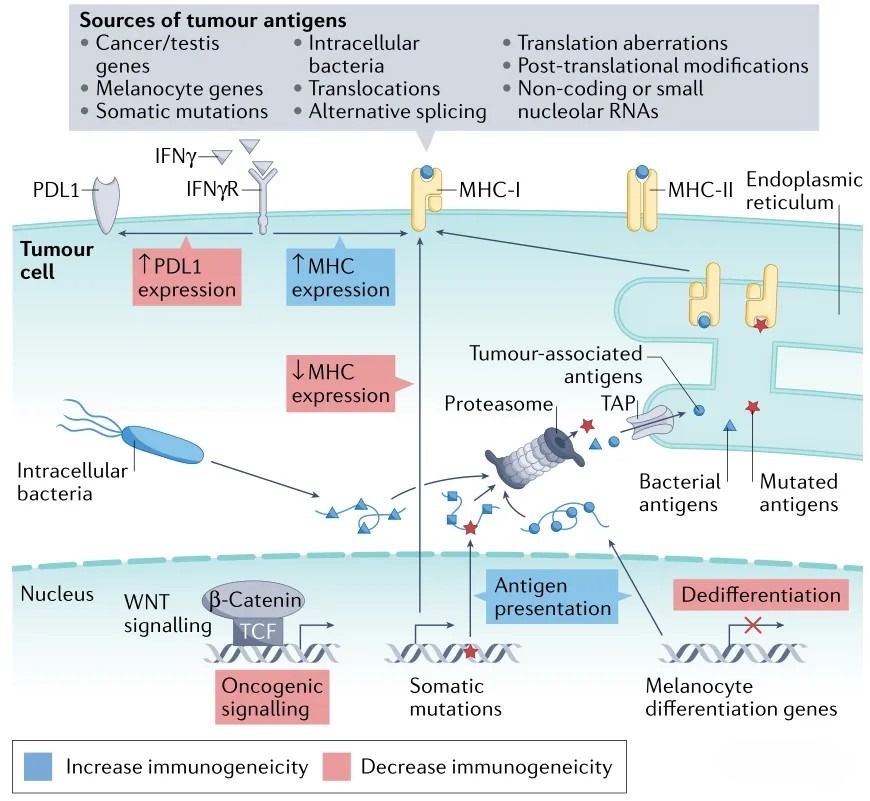 图4 肿瘤内在机制及其对肿瘤免疫反应的影响
图4 肿瘤内在机制及其对肿瘤免疫反应的影响
六、全文总结
深入理解肿瘤免疫学,关键在于阐明肿瘤与机体免疫系统之间的相互作用机制,尤其是肿瘤微环境中的免疫调控因素。近年来,关于癌细胞与免疫细胞之间相互作用的研究数量显著增长。单细胞多组学技术、基于人工智能的系统生物学方法以及基因编辑技术的迅速发展,极大