一、细胞因子概述
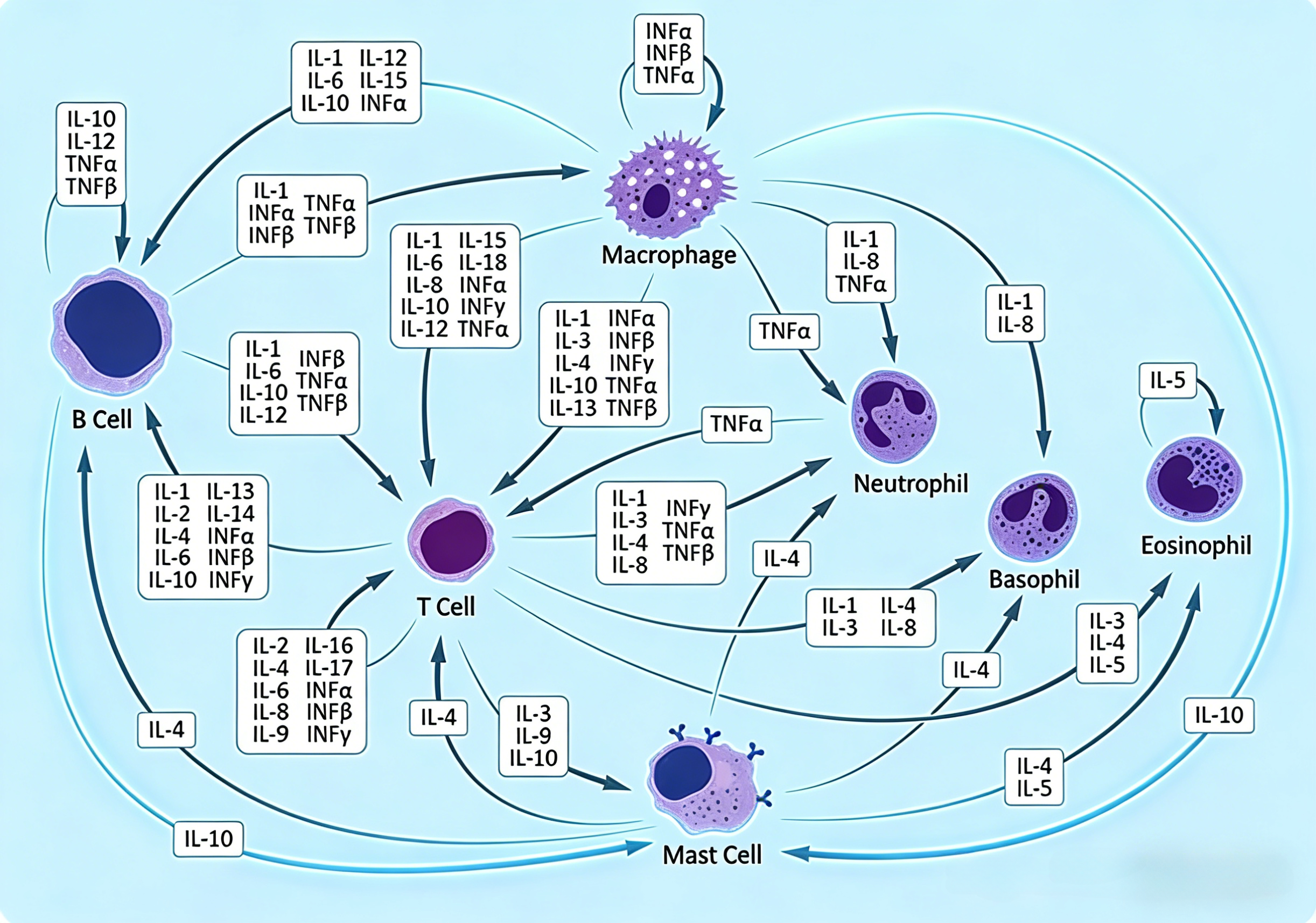
细胞因子是一类由免疫细胞(如单核细胞、巨噬细胞、T细胞、B细胞及自然杀伤细胞等)及部分非免疫细胞(如内皮细胞、表皮细胞、成纤维细胞等)在相应刺激诱导下合成并分泌的小分子蛋白质,具有广泛的生物学活性。
根据功能差异,细胞因子可分为促炎性细胞因子与抗炎性细胞因子两大类。促炎性细胞因子主要由Th1细胞、CD4+T细胞、巨噬细胞及树突状细胞分泌,代表性成员包括IL-1(IL-1α、IL-1β)、IL-2、IL-6、IL-8、IL-11、IL-12、IL-17、IL-18、IL-33、LIF、OSM、CNTF、TGF-β、GM-CSF、IFN-γ及TNF-α。其中,IL-1(IL-1α、IL-1β)、IL-6及TNF-α是最为关键的促炎性细胞因子。
这些促炎性细胞因子主要通过I型细胞因子受体传递信号,该受体在结构上区别于其他类型的细胞因子受体。它们精密调控细胞介导的免疫应答,在免疫系统的功能调节中发挥核心作用。具体而言,促炎性细胞因子可调节免疫细胞的生长、活化、分化及其向感染部位的迁移,从而有助于控制并清除细胞内病原体(包括病毒)。
抗炎性细胞因子则是一类调节并抑制促炎性细胞因子反应的免疫调节分子。它们与特定的细胞因子抑制剂及可溶性细胞因子受体协同作用,精细调控机体的免疫反应。抗炎性细胞因子在正常炎症反应中的生理功能,以及在全身性炎症状态下的病理意义,均已得到广泛认可。主要的抗炎性细胞因子包括IL-1受体拮抗剂、IL-4、IL-10及IL-13。
二、细胞因子检测技术概述
目前,检测细胞因子的方法多种多样,根据检测原理和技术手段的不同,可大致分为免疫学检测方法、分子生物学检测方法及质谱法等类别。其中,基于免疫学的检测技术发展迅速,应用广泛。
在免疫学检测方法中,细胞因子作为一类蛋白质抗原,能够与其特异性单克隆抗体发生结合,利用抗原-抗体反应实现对细胞因子的定性或定量检测。代表性的技术包括Luminex液相芯片检测技术、MSD超敏电化学发光技术、流式液相微球免疫分析技术(CBA)以及Olink高通量蛋白组学技术等。这些方法在灵敏度、多重检测能力和样本适用性方面各具优势,广泛应用于基础研究与临床检测。
分子生物学方法则主要检测细胞因子的基因表达水平,包括对DNA及mRNA表达水平的分析。对于表达水平较低或仅由极少量细胞产生的细胞因子,因其含量过低,常规免疫学或生物学方法难以准确测定。常用的分子生物学检测技术包括聚合酶链式反应、逆转录聚合酶链式反应、Southern印迹、Northern印迹、斑点印迹、原位杂交及原位PCR等。
三、Luminex液相芯片检测技术概述
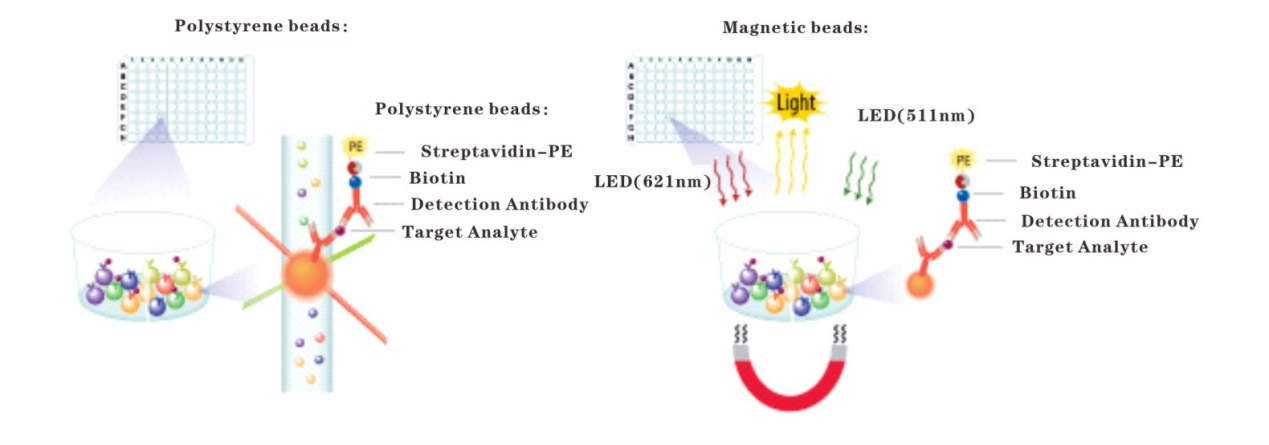
Luminex液相芯片技术是一种结合微球编码与流式细胞仪原理的蛋白检测方法。其核心技术在于利用荧光染料对聚苯乙/烯微球或磁性微球进行编码:通过调节两种荧光染料的不同配比,可制备出多达100种具有独特荧光光谱的微球,每种微球表面共价交联针对特定抗原的捕获抗体。
在实际应用中,将针对不同检测物的编码微球混合后,加入待测样本,样本中的靶分子与微球表面的捕获抗体发生特异性结合。每个反应孔中可同时完成最多100种检测反应。上机检测时,仪器通过两束激光分别识别微球的编码信息及其表面报告分子的荧光信号强度;其中荧光强度与微球结合的靶蛋白含量呈正相关,用于定量分析。因此,该技术可实现多样本中多个蛋白的同时检测。
Luminex技术类似于多重酶联免疫吸附测定,具备皮克级别的绝对定量能力。其可检测的靶标涵盖细胞因子、趋化因子、转录因子及生长因子等260余种蛋白,并可应用于数千种基因表达水平的分析。该技术的一大优势在于单次实验即可同时检测多种蛋白指标。
四、MSD超敏电化学发光技术概述
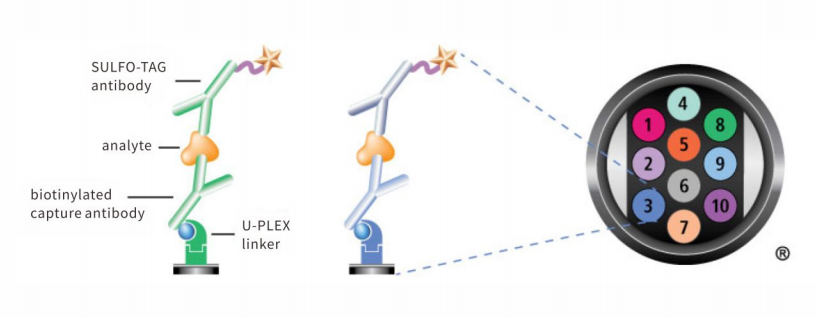
超敏电化学发光技术是一种基于石墨微孔板的电化学发光免疫分析方法。该技术是在酶联免疫吸附测定基本原理上的升级,通过在板底通电,激发标记物(SULFO-TAG)产生电化学发光信号,并利用电荷耦合器件相机进行信号采集。
在检测平台方面,该系统可采用基于点阵技术的96孔石墨电极板,每个反应孔中最多可同时检测10个指标;亦可在24孔板中实现定制化检测,每孔最高可完成100个指标的筛选分析。
该技术的检测灵敏度略高于流式细胞术检测系统,能够定量检测生理状态下的多种天然细胞因子(如IL-6、IL-8、IL-10、TNF-α、IL-12p70、IL-1β)的循环水平,并可准确回收添加到血清样本中的已知浓度重组细胞因子。
作为一种电化学发光检测方法,该技术适用于细胞因子、蛋白质、抗体及核酸等生物分子的分析,属于第三代免疫分析技术。
五、微球免疫分析技术概述
微球免疫分析技术,又称流式编码微球芯片技术或细胞因子微球检测技术,是一种利用流式细胞仪对多重蛋白进行定量检测的方法。该技术能够同时对样本中的多个指标进行定性与定量分析,广泛应用于细胞因子检测领域。
该技术基于流式细胞术的原理,采用微米级荧光标记微球。每种微球表面携带针对特定细胞因子的特异性抗体,这些抗体可与待测样本中相应的细胞因子结合。不同检测指标的微球具有不同的荧光信号,以便后续流式细胞仪进行识别和区分。
检测过程中,将多种编码微球混合后加入待测样本,样本中的目标细胞因子或蛋白质与微球表面的相应抗体特异性结合,形成免疫复合物。通过洗涤步骤去除未结合的成分,确保仅保留与抗体结合的微球。随后加入荧光标记的二抗,二抗与免疫复合物中的抗体结合,从而标记被检测的分子。处理后的微球与样本混合液经流式细胞仪分析,通过测量每个微球的荧光强度,可确定样本中特定蛋白质或细胞因子的浓度。
该技术的主要优势在于能够同时进行多参数检测,具有检测速度快、信息量大的特点。此外,其可在单个样本中同时完成多项指标检测,所需样本量少、灵敏度高、稳定性好。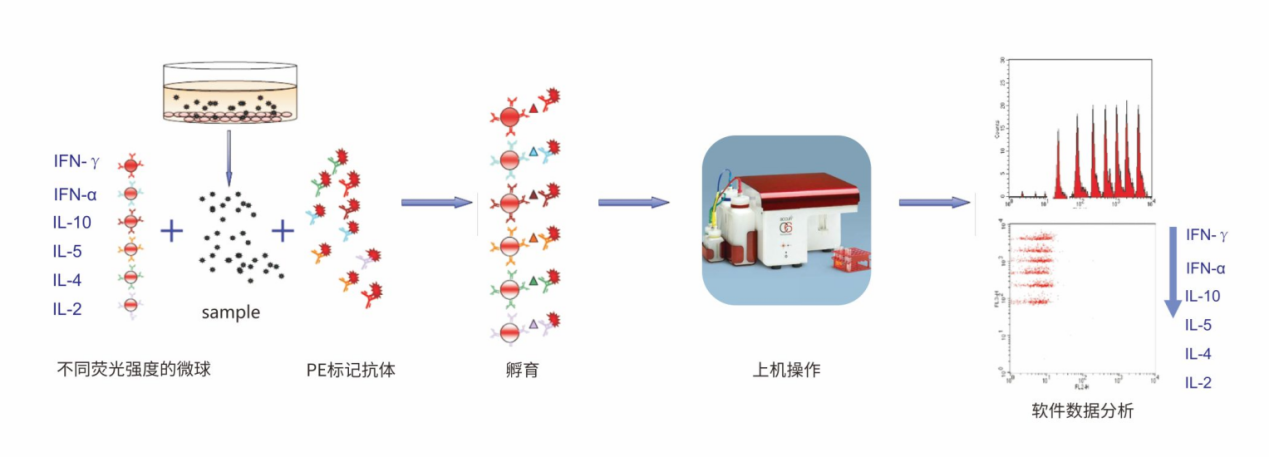
六、高通量蛋白组学(Olink)技术概述
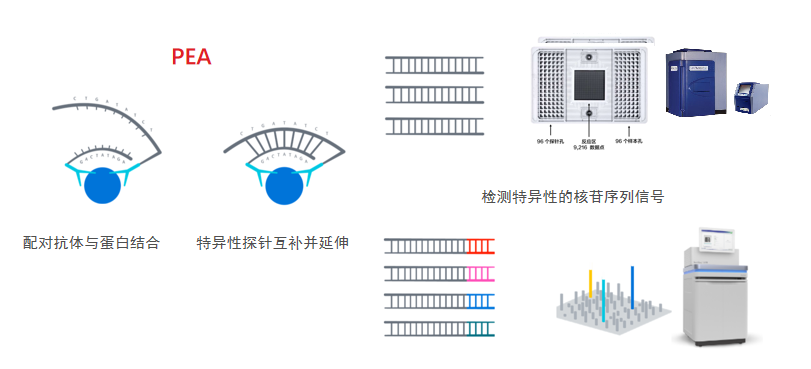
Olink技术是一种基于邻近延伸分析原理的高通量蛋白组学检测方法,广泛应用于细胞因子及多种炎症相关蛋白的定量分析。该技术结合了抗体免疫识别与核酸扩增检测的优势,能够在微量样本中实现高灵敏度、高特异性的多重蛋白检测。
在技术原理上,Olink方法采用成对的抗体,每个抗体分别偶联一条独特的DNA寡核苷酸链。当这两条抗体同时与目标蛋白分子上的相邻表位结合时,所携带的DNA链在空间上相互靠近,从而发生杂交并作为模板进行后续的延伸反应。通过实时定量聚合酶链反应或微流控芯片技术对延伸产物进行定量检测,可间接反映样本中目标蛋白的浓度。
Olink技术具有极低的检测下限,可达到飞克级别,尤其适用于低丰度蛋白(如多种细胞因子、趋化因子和生长因子)的检测。该技术所需的样本量极少,通常仅需数微升体液或少量细胞裂解物,即可同时检测数十至数百种蛋白指标。此外,其检测动态范围宽,可覆盖内源性蛋白在生理及病理状态下的广泛浓度变化。
在细胞因子研究领域,Olink技术能够实现对炎症反应、免疫调节及相关信号通路中关键蛋白的系统性筛查,具有高通量、高重复性和良好的批次间稳定性,是继传统免疫检测方法之后的重要技术补充。
七、总结
综上所述,细胞因子作为免疫系统中关键的信号分子,其促炎与抗炎两大类型的平衡在机体免疫调节中发挥核心作用。为准确检测细胞因子的表达水平及功能状态,现已发展出多种检测技术。其中,基于抗原-抗体反应的免疫学方法(如Luminex、MSD、CBA及Olink等)因具备高灵敏度、高通量及多重检测能力,已成为当前细胞因子研究的核心技术手段。不同技术在检测原理、动态范围、样本需求量及多重检测能力方面各有特点,研究者可根据具体实验需求选择适宜的方法。随着蛋白组学技术的不断进步,细胞因子检测正朝着更高灵敏度、更宽检测范围及更高通量的方向发展,为免疫相关疾病的机制研究及临床诊断提供重要支撑。