上海乐备实生物技术有限公司品牌商
6 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
公司新闻/正文
在肠道疾病的发生发展中,共生关系的稳定起到多少决定性作用?
612 人阅读发布时间:2021-12-07 11:23
共生关系通过宿主对微生物因素的持续感知和耐受性或促炎反应的产生而得以维持。

加速 T 细胞转移结肠炎病理
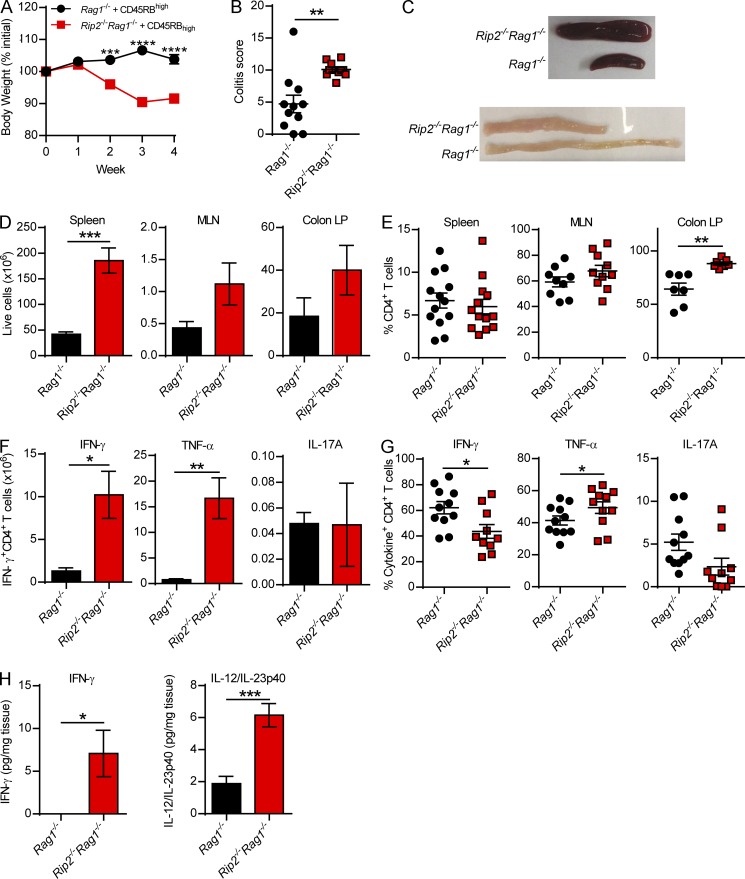
不受调节细胞的保护
将 CD4 + CD45RB LowT 细胞共同转移到Rip2 -/-Rag1 -/-小鼠中并不能保护小鼠免受结肠炎的侵害。这些小鼠的脾脏细胞数量仍然增加,结肠 LP 和肠系膜淋巴结的CD4 + T 细胞浸润增加。在结肠中仍观察到IFN-γ + CD4 + T 细胞和 TNFα + CD4 + T 细胞数量的增加,以及结肠 IFN-γ 和 IL-12/IL-23p40 蛋白的增加。各种其他细胞因子,例如 IL-1β、IL-6、IL-10、IL-12p70、IL-13、KC、MIP-1α 和 MIP-2 在Rip2 -/-Rag1 -/-结肠中也增加。
结果提示:Rip2 -/- Rag1 -/-小鼠中促炎介质的早期增加可能会阻断 CD4 + CD45RB T 细胞抑制炎症的能力。
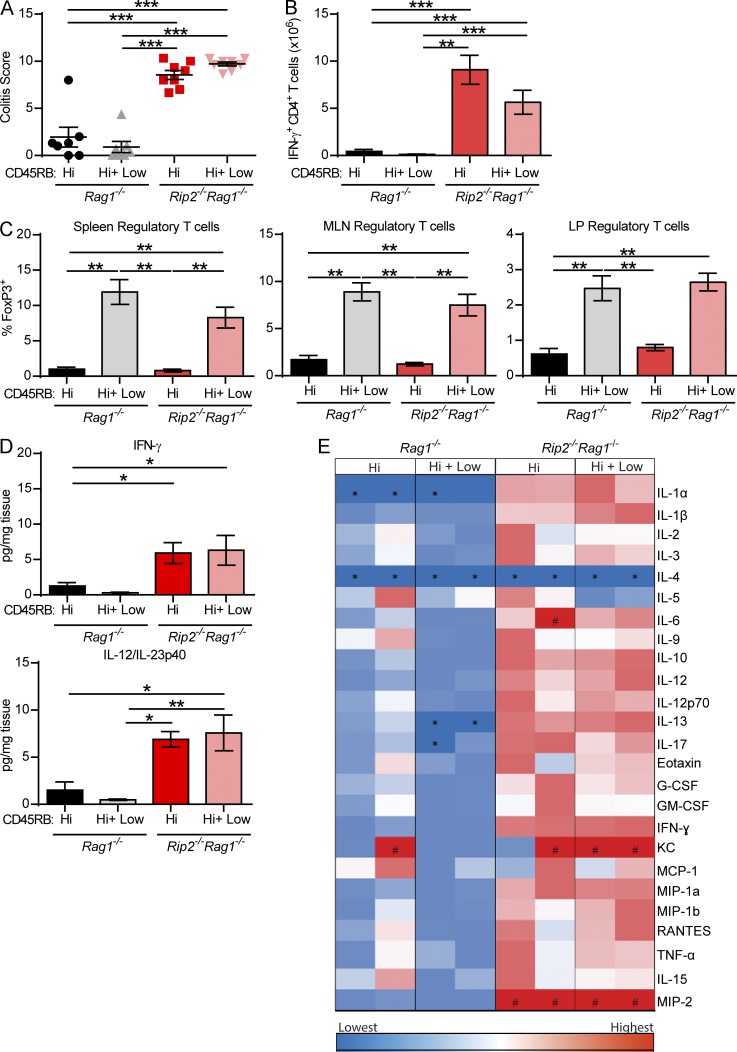
具有传染性特点
Rip2 -/- Rag1 -/-和Rag1 -/-小鼠经共同的断奶时笼养,5 周后注射 CD4 + CD45RB T 细胞。转移 4 周,共笼Rag1 -/-小鼠出现与Rip2 -/- Rag1 -/-小鼠表现出相同的病理学加剧现象,表明致病因子可以横向转移。然后生成同窝小鼠,由此产生的Rip2 +/+ Rag1 -/-小鼠也发展为加速结肠炎,并且具有与其Rip2 -/-Rag1 -/-同窝小鼠相似的促炎细胞因子水平。
结果提示:导致Rip2 -/- Rag1 -/-小鼠结肠炎恶化的主要原因为微生物因素,而不是Rip2基因型。对Rip2 -/-Rag1 -/-和Rag1 -/-非同窝小鼠和同窝小鼠进行病毒感染筛选,结果也提示MNV 感染不是 T 细胞转移结肠炎的主要因素。
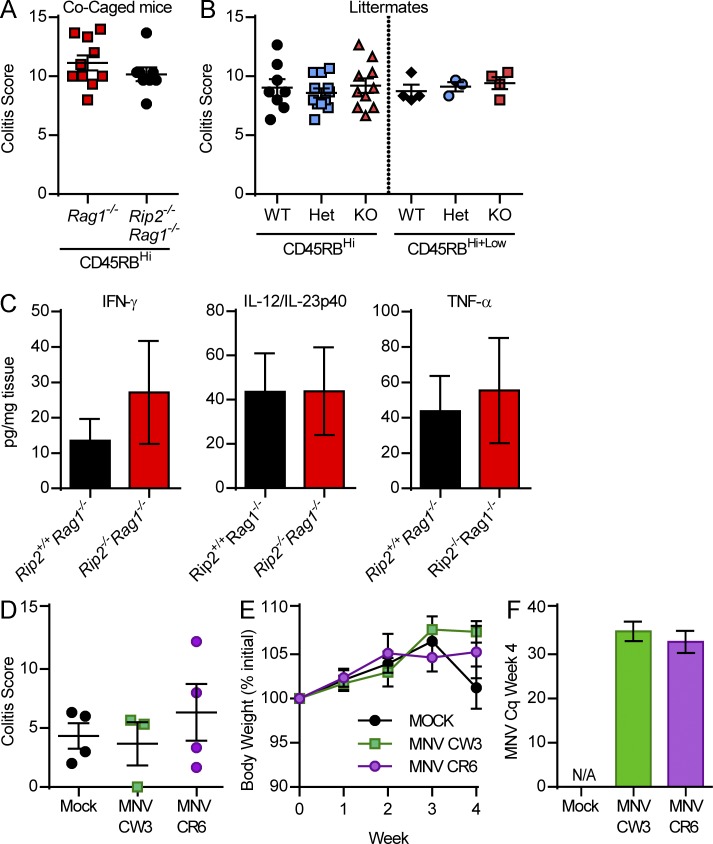
T. muris感染加剧 T 细胞转移性结肠炎
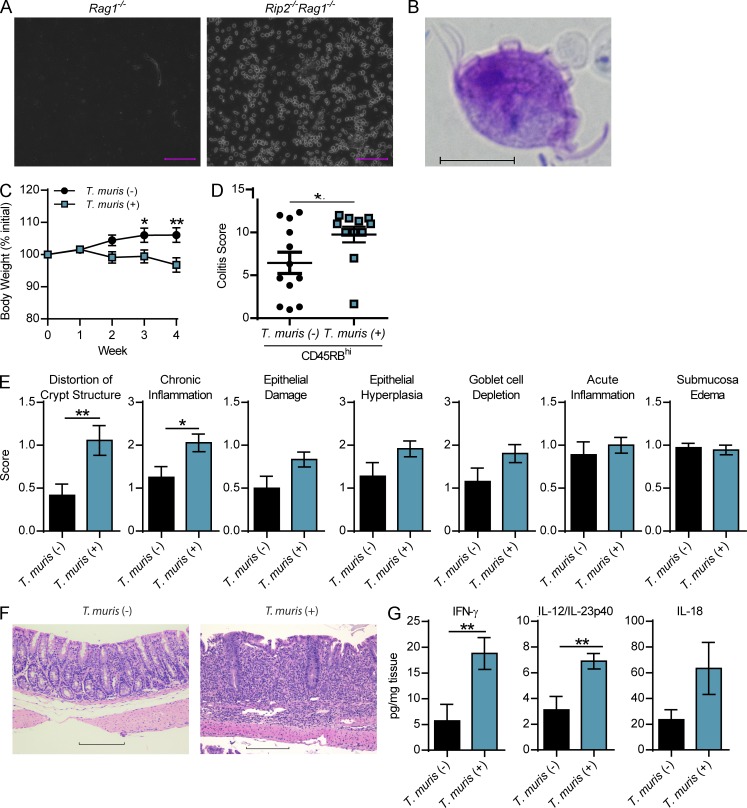
T. muris从Rip2 -/- Rag1 -/-小鼠的盲肠内容物中分离出来并口服灌胃给Rag1 -/-小鼠。2 周后,CD4 + CD45RB高T 细胞被转移到T. muris感染的Rag1 -/-小鼠及其未感染的同窝小鼠对照中。在 T 细胞转移后 4 周,T . muris感染的小鼠比它们的模拟攻击的兄弟姐妹减轻了更多的体重。在T.缪里斯感染的小鼠具有增加显著隐窝结构的损失,上皮损伤(P = 0.0545),和淋巴细胞浸润。受感染小鼠结肠中的 IFN-γ 和 IL-12/IL-23p40 蛋白水平也升高,而 IL-18 没有显着升高。总之,这些数据表明,T. muris感染导致结肠中升高的 Th1 促炎环境,导致 T 细胞转移结肠炎期间结肠病理增加。
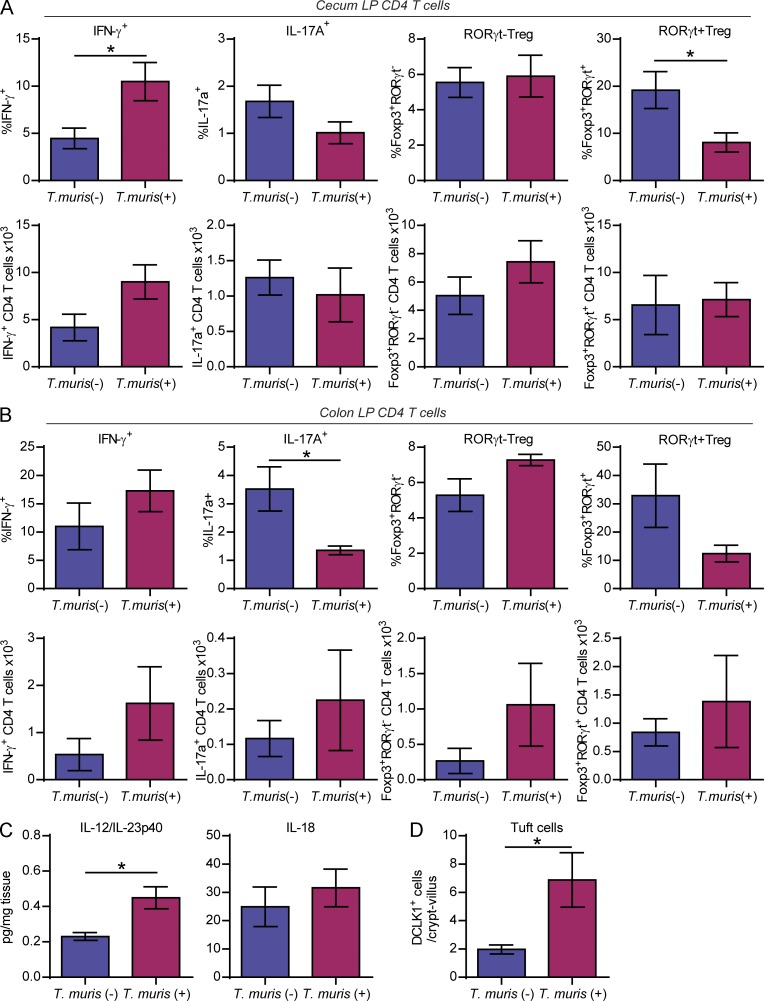
慢性 T. muris感染改变基线 T 细胞稳态
受感染小鼠的盲肠 LP中 IFN-γ + CD4 T 细胞的频率和数量(P = 0.0617)有增加的趋势。相反,结肠 LP中 IL-17A + CD4 T 细胞的频率降低。Rorγt - Foxp3 + Treg 细胞频率和数量在感染和未感染小鼠之间无差异,但 Rorγt + Foxp3 + T reg 细胞频率降低。在培养的结肠外植体上清液中,IFN-γ 蛋白水平低于检测水平,IL-18 没有显着差异,但IL-12/IL-23p40 蛋白在T. muris定植小鼠中升高。IL-12/IL-23p40 蛋白和产生 IFN-γ 的 CD4 T 细胞的基线增加,伴随着 T reg 细胞的减少。
结果提示:T 细胞转移结肠炎期间Rip2 -/- Rag1 -/-结肠中的多种细胞因子增加表明T. muris可能充当一般刺激物粘膜免疫系统,而非 Th1 反应。
结论
小鼠急性感染与相关原生动物T. musculis诱导 IL-18 驱动的 Th1 和 Th17 反应,这些反应改变了细菌诱导的结肠炎、T 细胞驱动的结肠炎和结直肠肿瘤形成的结果。研究还表明原生动物感染后 Th1 反应增加,但 IL-18 和 IL-17 水平并未显着增加。这种差异可能是慢性与急性感染的结果或不同原生动物的结果。
尽管T. muris与肠道内细菌之间的关系尚不清楚,但T. muris的盲肠内容物中存在大量原生动物定植的小鼠表明可能对细菌组成产生影响。因此,除了寻找潜在的T. muris特异性抗原外,还可以探索T. muris诱导的细菌生态失调的潜力。
讨论
虽然T. muris现在可能被标记为肠道疾病模型中的潜在混杂因素,但它是否会影响全身性疾病仍有待确定。此外,仍然存在许多其他未鉴定的原生动物或微生物,它们也可能在小鼠模型中发挥免疫调节作用,且该研究也警示研究者们在进行动物模型构建时需要适当的同窝对照实验。
详见LabEx网站( http://www.u-labex.com)或来电咨询!
基因水平:PCR Array
蛋白水平:MSD、Luminex、CBA、Antibody Array、ELISA
细胞水平:磁珠分选、流式细胞分析
组织水平:多重免疫组化、病理分析
联系电话:4008-168-068 转3
联系邮箱:labex@univ-bio.com
公众平台:多因子实验服务专家


