上海乐备实生物技术有限公司品牌商
6 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
公司新闻/正文
穿越呼吸系统炎症分型迷雾!多因子名侦探已上线!
206 人阅读发布时间:2026-04-15 16:47
在呼吸系统疾病的研究领域,一个认知升级正在发生——过去,我们只需要证明“有炎症”。
现在,越来越多研究开始强调——炎症分型。
同样是炎症指标升高:
有的是 Th1 驱动的免疫激活;
有的是 Th2 主导的过敏性应答;
有的是 Th17 参与的中性粒细胞炎症;
有的则是免疫抑制主导的“冷”微环境;
如果不做分型,机制难以厘清,药效也无法真正解释透彻。这正是为什么,多因子检测在呼吸系统研究中,正从“加分项”走向“必选项”。
一、什么是呼吸系统炎症分型?
简单来说,炎症分型的核心不是看炎症指标“高不高”,而是看炎症背后“谁在主导”。同样是呼吸系统炎症,其背后的免疫逻辑可能存在天壤之别,而分型的意义,就在于揭示这种免疫反应的“结构差异”。
以感染模型为例,IL-6、TNF-α 升高,只能说明炎症强度在增强,但无法判断炎症的主导类型;但如果同时观察到 IFN‑γ、CXCL10 上升,则提示炎症更偏向 Th1 驱动;若看到 IL‑4、IL‑5、IL‑13 上升,则更可能是 Th2 倾向的炎症。这种通过多指标组合判断炎症类型的方式,就是炎症分型的核心逻辑。
二、为什么呼吸系统尤其需要分型?
呼吸系统的自身特点,决定了其炎症反应的复杂性,也让分型变得尤为必要。呼吸系统主要有三大特点:
一是开放性强,病原、过敏原、环境刺激等长期存在,易引发各类炎症;
二是免疫反应复杂,感染、过敏、组织重塑等过程往往同时存在,相互影响;
三是动态变化明显,炎症在不同时间阶段的表现差异显著,时间维度至关重要。
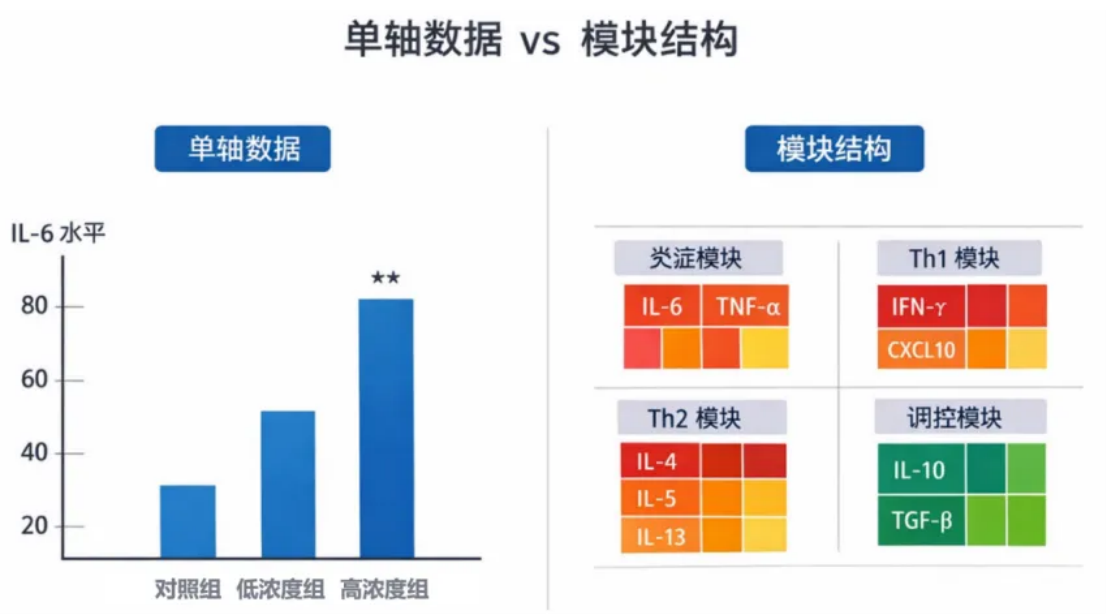
在这样的背景下,单一维度的检测数据很难清晰阐释免疫反应的整体结构。尤其是在哮喘分型、慢性炎症向纤维化转化、肺癌免疫微环境分析及新药药效评价等研究中,分型能力直接决定了研究的深度和准确性,是解锁呼吸系统炎症机制的关键。
三、单维检测为什么越来越难支撑分型?
单个炎症因子,本质上只代表一条免疫轴线,无法反映免疫反应的全貌。而炎症分型,至少需要同时观察三个核心维度:炎症强度轴、免疫分型轴、调控反馈轴。
如果仅依靠单维检测,缺乏横向的多指标对比,就很难回答核心问题:炎症的增强是驱动因素导致,还是调控机制减弱引起?是炎症单纯放大,还是免疫体系出现失衡?这也是为什么越来越多的科研研究,开始采用“模块化结构”的多因子检测,以此弥补单维检测的局限性。
四、多因子检测的真正价值:不在“多”,而在构建结构
很多人误以为多因子检测的价值在于“检测指标多”,实则不然。其核心价值在于通过多指标的组合,构建出完整的免疫反应结构,为炎症分型提供有力支撑。
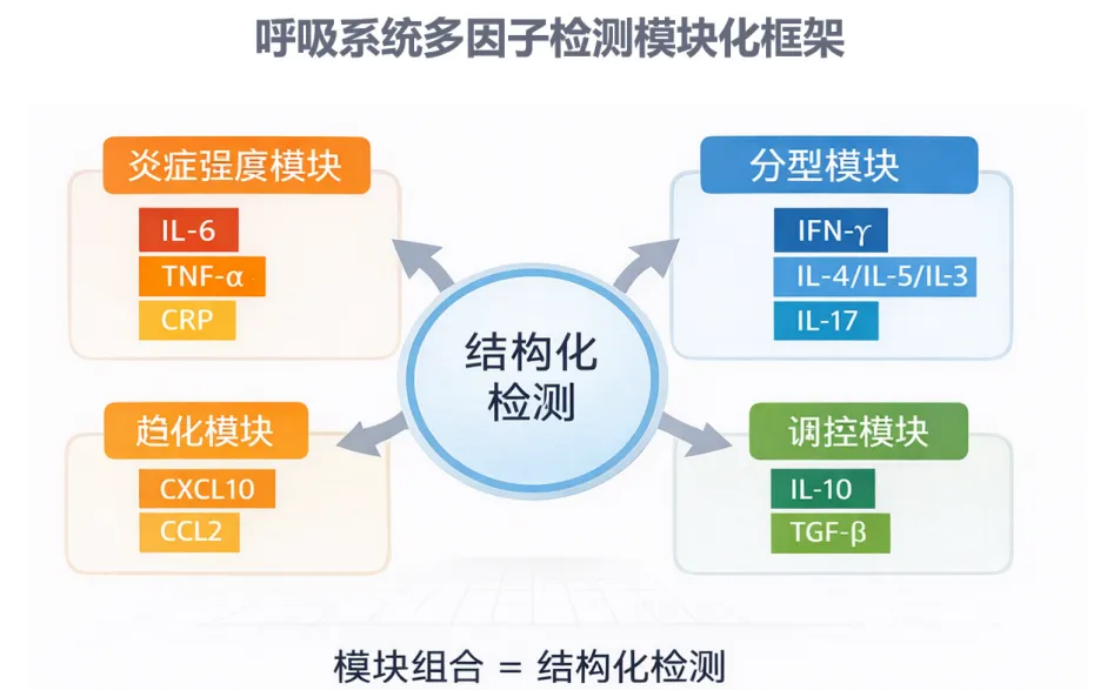
从科研角度来看,多因子检测能提升炎症机制的解释力,帮助研究者更清晰地梳理免疫反应的内在逻辑;
从工业角度而言,它能增强新药药效与风险评估的结构性,让评估结果更全面、更可靠。
如今,多因子检测成为科研与工业领域的“标配”,并非单纯的流行趋势,而是支撑炎症分型、推动研究与应用落地的必要手段。
五、下一步:如何按研究方向设计分型模块?
炎症分型并非“一刀切”,不同的研究方向,其分型逻辑和检测重点完全不同。例如,感染模型的研究重点关注 IFN 轴相关指标,以此判断感染引发的免疫反应类型;哮喘研究则聚焦 Th2 轴,解析过敏相关的炎症机制;肿瘤微环境研究重点关注免疫抑制轴,探索肿瘤进展与免疫调控的关系;药物研发则更关注炎症结构的变化与安全信号,为药物有效性和安全性提供数据支撑。
六、如果要做多因子检测,高分文章到底是怎样设计panel的呢?
真正拉开研究差距的,不仅是测多少因子,更重要的是panel的组合设计。
1、感染与急性炎症研究:重点看 “免疫反应结构”
在病毒感染、细菌感染、急性肺损伤(ALI)以及 ARDS 研究中,研究重点从来不是单纯的炎症指标升高,而是免疫反应是否失衡。
在严重呼吸道感染中,常见特征为 IFN-γ、TNF-α、CXCL10 等因子共同驱动炎症型巨噬细胞状态,且与疾病严重程度直接相关;同时,重症肺炎患者中 IL-6、IL-8、TNF-α、IL-10 等多种细胞因子显著升高,形成典型的炎症因子网络。
越来越多研究聚焦一个核心问题:这是一场正常免疫反应,还是正在发展为炎症风暴?因此,研究中可通过同时检测四大模块,完整解析免疫反应结构:
l 炎症强度模块:IL-6、TNF-α、IL-1β
l 抗感染免疫模块:IFN-γ、IFN-α、CXCL10
l 趋化模块:MCP-1、IL-8、MIP-1α
l 免疫调控模块:IL-10、IL-1RA

2、哮喘与过敏性炎症研究:核心是 Th2 分型
在呼吸系统疾病研究中,哮喘始终是高关注度领域。近年来大量研究明确:哮喘是一种免疫分型疾病,核心可分为 Type 2-high 与 Type 2-low 两大类型。
目前临床与研究普遍认为,IL-4、IL-5、IL-13 是驱动哮喘的关键 Th2 细胞因子,也是生物制剂治疗的核心靶点。因此,多因子检测 panel 需围绕 Th2 免疫轴展开,精准实现哮喘分型。
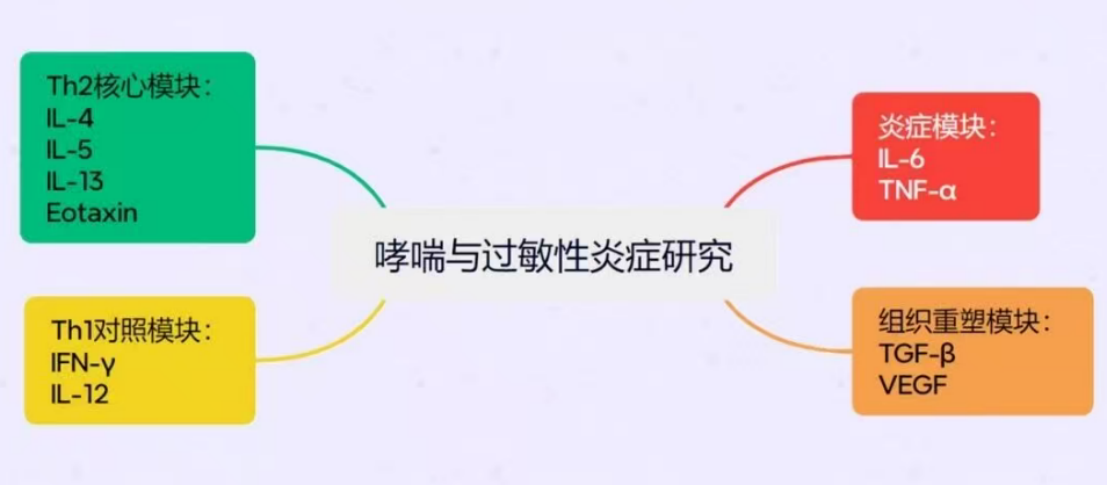
研究的核心关注点是:免疫偏移如何推动哮喘分型与疾病进展?为此,可通过四大模块构建完整检测体系:
l Th2 核心模块:IL-4、IL-5、IL-13、Eotaxin
l Th1 对照模块:IFN-γ、IL-12
l 炎症模块:IL-6、TNF-α
l 组织重塑模块:TGF-β、VEGF
3、慢性炎症与纤维化研究:炎症如何推动结构改变
在 COPD、肺纤维化以及慢性炎症模型研究中,研究重点并非炎症本身,而是炎症是否正在推动组织结构改变。例如在特发性肺纤维化研究中,IFN-γ、CCL2、CXCL10 等多种炎症与趋化因子,被证实与疾病急性加重及预后密切相关。
当前研究的核心方向是:慢性炎症如何逐步演变为组织重塑与纤维化?因此,多因子 panel 设计需覆盖四大核心模块,追踪炎症向纤维化的转化过程:
l 慢性炎症模块:IL-6、TNF-α、IL-1β
l 组织重塑模块:TGF-β、PDGF、FGF
l 趋化模块:CCL2、CCL3
l 血管生成模块:VEGF

4、肺癌免疫微环境研究:免疫激活 vs 免疫抑制
随着免疫治疗的快速发展,肺癌研究的核心逐渐转向肿瘤免疫微环境(TME)。近年研究表明,在炎症性疾病中,IFN-γ 与 TNF-α 可诱导 CXCL10 + 炎症型巨噬细胞,这种免疫状态同样在肿瘤微环境中广泛存在。
研究的关键问题是:肿瘤微环境中,免疫系统是被激活,还是被压制?为此,多因子 panel 需围绕免疫平衡设计四大模块,全面解析 TME 特征:
l 免疫激活模块:IFN-γ、IL-2、Granzyme B
l 免疫抑制模块:IL-10、TGF-β、IL-35
l 炎症模块:IL-6、TNF-α
l 趋化模块:CXCL9、CXCL10、CCL5

5、药物研发与机制研究:多因子检测正在成为标配
随着免疫治疗的发展,肺癌研究的重点逐渐转向肿瘤免疫微环境(TME)。近年研究证实,炎症性疾病中 IFN-γ 与 TNF-α 诱导的 CXCL10 + 炎症型巨噬细胞状态,同样广泛存在于肿瘤微环境中。
在药物研发领域,越来越多研究开始用多因子数据回答核心问题:药物为什么有效,而不仅仅是是否有效。多因子检测已从 “可选项” 变为 “标配”,通过四大模块实现药效与安全性的全面评估:
l 炎症模块:IL-6、TNF-α、IL-1β
l 免疫分型模块:IFN-γ、IL-4、IL-17A
l 安全性信号模块:IL-10、GM-CSF
l 趋化模块:MCP-1、IL-8

核心总结
呼吸系统炎症的本质是免疫结构的差异,而非单一指标的高低。不同研究方向对应完全不同的分型逻辑:感染看免疫失衡、哮喘看 Th2 分型、纤维化看结构重塑、肺癌看免疫平衡、药物研发看机制与安全。多因子检测的核心价值,正是通过模块化设计,为不同研究方向构建精准的免疫结构解析体系,全面提升研究深度与转化价值。


