一、引言
脂质作为机体主要能量储备与生物膜结构成分,参与激素合成、信号传递与炎症调控。脂代谢以脂肪酸为核心底物,在肝脏、脂肪组织、骨骼肌等器官协同完成,其稳态失衡是代谢综合征的共同病理基础。近年来,脂滴生物学、脂肪因子功能与组织特异性代谢调控成为研究热点,揭示了脂代谢网络在疾病发生中的关键作用。本文整合脂质摄入利用、脂肪从头合成、脂肪动员、细胞因子与信号通路等层面,全面阐述脂代谢的分子机制与调控逻辑。
二、脂质的摄入、转运与细胞利用
外源性脂质以三酰甘油(TAG)为主要形式,占膳食脂质90%,辅以磷脂、胆固醇与游离脂肪酸。
脂质经消化吸收后由血浆脂蛋白转运,包括乳糜微粒(CM)、极低密度脂蛋白(VLDL)、低密度脂蛋白(LDL)与高密度脂蛋白(HDL),实现脂质在组织间的分配运输。 循环TAG经脂蛋白脂酶(LPL)水解生成脂肪酸(FA),FA通过被动扩散或CD36、FATP、FABP等转位酶进入细胞。胞内FA经长链脂肪酰基辅酶A合成酶(ACSL)活化为酰基辅酶A,一部分进入脂滴储存,另一部分经肉碱棕榈酰转移酶1(CPT1)转运至线粒体进行脂肪酸氧化(FAO),通过三羧酸循环(TCA)生成ATP;TCA产生的柠檬酸可出线粒体转化为乙酰辅酶A,启动脂肪从头合成,实现能量储存与利用的动态平衡。
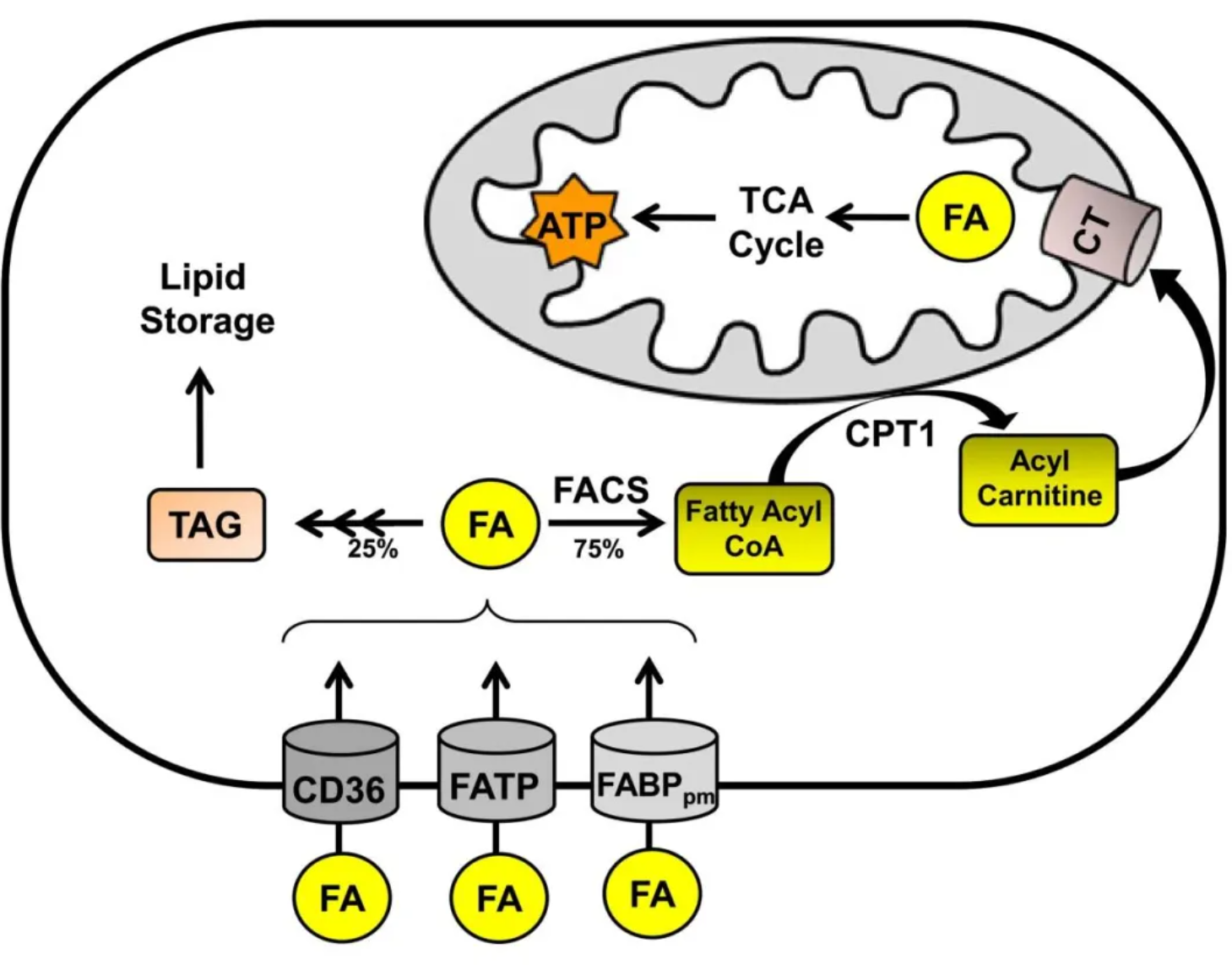
图1. 脂肪酸(FA)代谢示意图
三、脂肪从头合成(DNL)的分子途径
脂肪从头合成是将碳水化合物、氨基酸等非脂前体转化为TAG的过程,主要发生于肝脏与脂肪组织,是能量过剩时脂质储存的核心通路。饱食状态下,糖代谢与氨基酸代谢提供乙酰辅酶A,在ATP柠檬酸裂解酶(ACLY)、乙酰辅酶A羧化酶1(ACC1)催化下生成丙二酰辅酶A,经脂肪酸合成酶(FASN)合成软脂酸,再由脂肪酸延长酶6(ELOVL6)与硬脂酰辅酶A去饱和酶(SCD)生成长链不饱和脂肪酸,最终组装为TAG储存于脂滴。 脂肪组织以葡萄糖为主要原料,经GLUT4/GLUT1转运进入细胞,通过糖酵解与TCA循环提供柠檬酸,支持DNL进程;同时可利用CM/VLDL来源的脂肪酸合成TAG,实现外周能量储备。肝脏DNL异常活跃是高糖膳食诱导脂肪肝的重要分子机制。
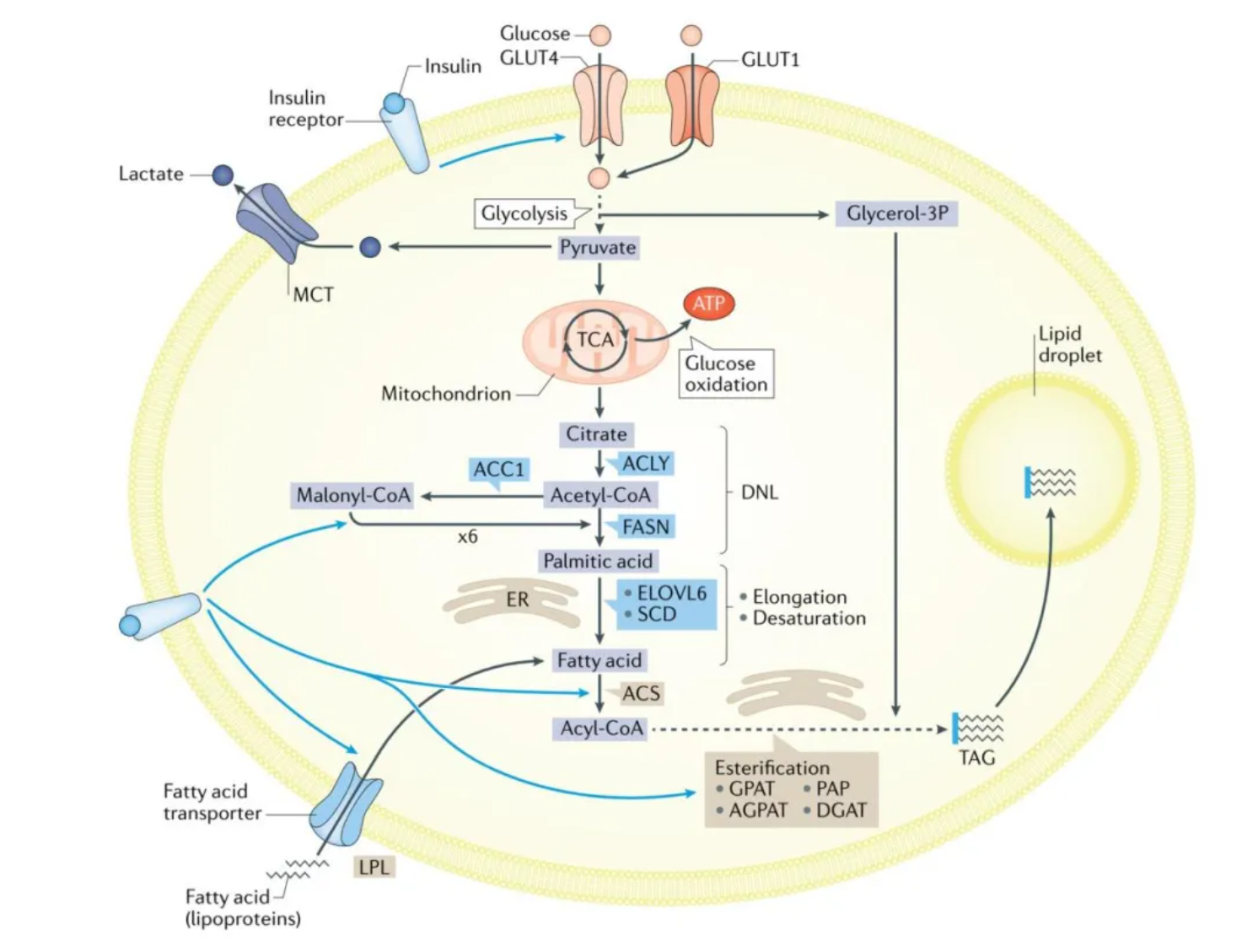
图2. WAT中的脂肪储存与葡萄糖代谢
四、脂肪动员与脂质分解代谢
脂肪动员是能量匮乏(禁食、运动)时,脂肪细胞TAG水解释放游离脂肪酸(FFA)与甘油的过程,由三种中性脂肪酶有序催化:
1.甘油三酯脂肪酶(ATGL):水解TAG生成二酰甘油(DAG);
2.激素敏感脂肪酶(HSL):水解DAG生成单酰甘油(MAG),参与多步脂质水解,为限速酶;
3.单甘酯脂肪酶:水解MAG生成甘油与脂肪酸。 释放的FA经血液循环至肝、肌、心等组织,进入线粒体氧化供能。脂代谢合成与分解受转录因子精准调控:SREBP主导脂质合成,PPAR主导脂质分解,共同维持全身脂质稳态。
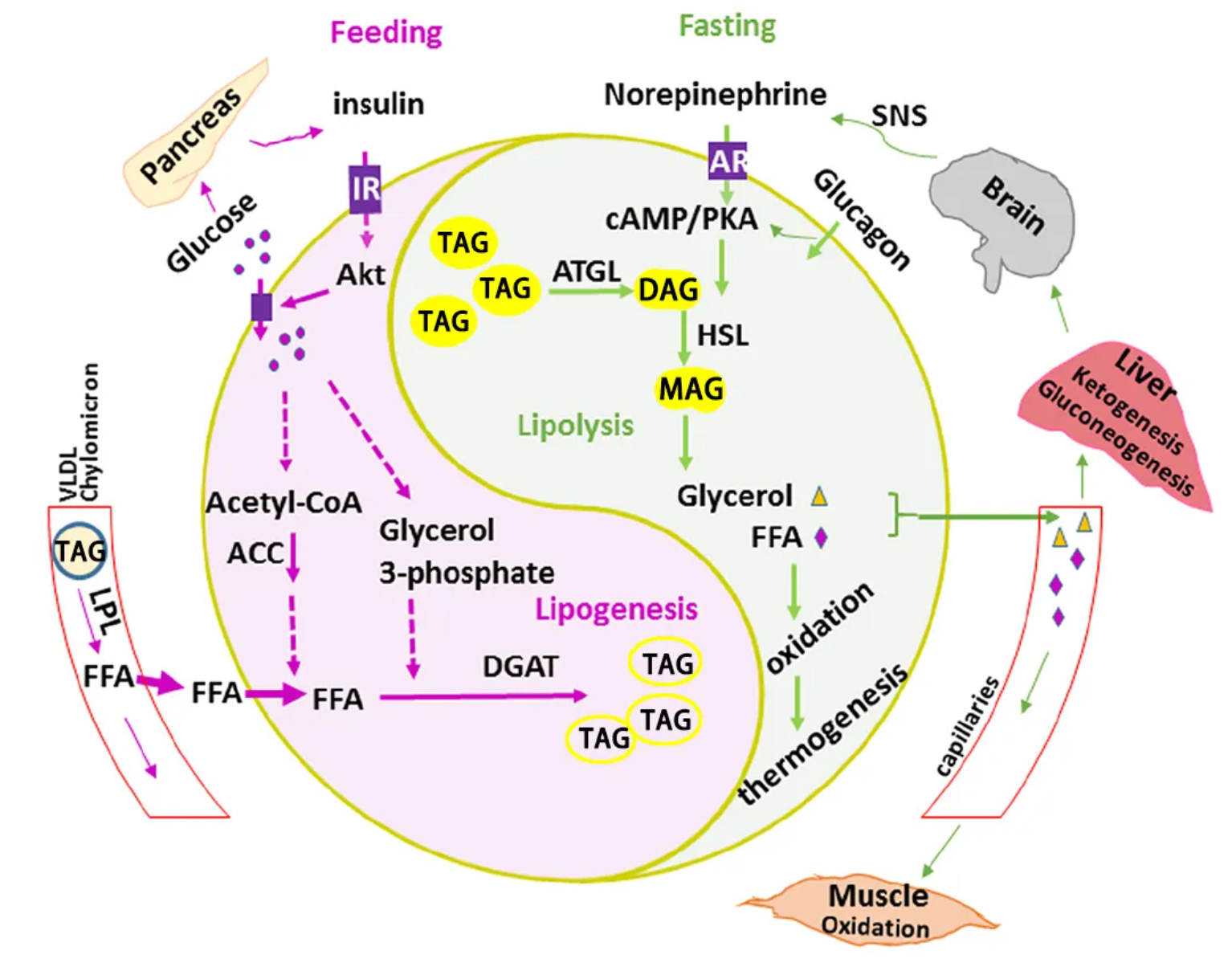
图3. 脂质代谢和动员
五、脂肪因子与代谢炎症调控
脂肪组织作为内分泌器官,分泌多种脂肪因子参与代谢调控,肥胖状态下因子分泌紊乱,驱动代谢炎症与胰岛素抵抗。
- 脂联素:脂肪细胞特异性分泌,增强胰岛素敏感性,抑制肝糖异生,促进骨骼肌脂肪酸氧化,具备抗糖尿病、抗动脉粥样硬化与抗炎活性,骨骼肌、心肌、肝细胞亦可少量分泌;
- 瘦素:调节食欲、能量消耗、骨量与胰岛素分泌,肥胖者常出现瘦素抵抗;
- 正常脂肪细胞分泌脂联素、SFRP5等抗炎因子;肥胖病理状态下,TNF-α、IL-6等促炎因子上调,诱发代谢炎症与组织损伤。
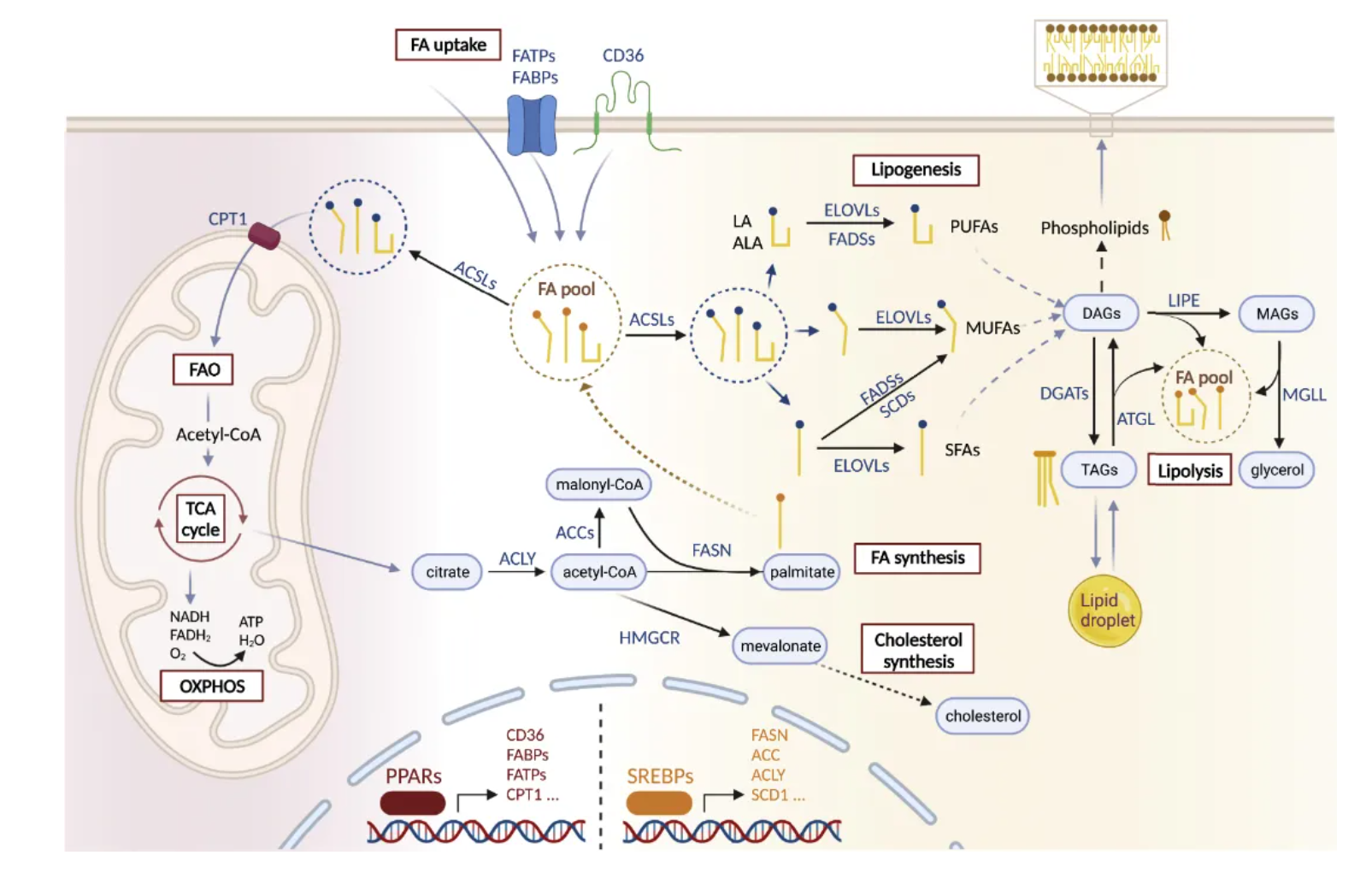
图4. 主要脂代谢途径
六、脂联素组织特异性信号通路
脂联素通过AdipoR1/AdipoR2受体激活下游信号,在骨骼肌、心肌、肝脏发挥组织特异性代谢调控作用。
(一)骨骼肌
脂联素激活APPL1介导AMPK与MAPK-PPARα通路,增强CPT1、ACOX1表达,促进脂肪酸氧化;同时激活PGC1α促进线粒体生物合成,介导GLUT4转位提升葡萄糖摄取,改善胰岛素敏感性。
(二)心肌
脂联素通过LKB1-AMPK通路抑制心肌肥大,激活eNOS减轻炎症与氧化应激,预防心肌梗死;激活PPARγ提升自身转录,增强心肌脂代谢稳态,保护糖尿病心肌病。
(三)肝脏
脂联素激活AMPK抑制SREBP1c,下调ACC、FAS、SCD1以减少脂质合成;解除ACC对CPT1的抑制,增强脂肪酸氧化;同时提升抗氧化酶水平,抑制TNF-α、MCP1等促炎因子,保护肝细胞免受脂毒性损伤。
七、总结与展望
脂代谢是多器官、多分子协同的精密网络,涵盖脂质摄取、转运、从头合成、储存、动员与氧化分解,受酶、转录因子与脂肪因子层级调控。脂联素-AMPK、SREBP、PPAR等通路是维持代谢稳态的核心节点,其异常驱动肥胖、糖尿病、脂肪肝等疾病。 未来研究应聚焦:
①脂滴动态调控与细胞器互作机制;
②组织特异性脂代谢重编程在疾病中的作用;
③脂肪因子-炎症-代谢轴的靶向干预;
④新型脂代谢标志物与药物靶点筛选。深入解析脂代谢网络,可为代谢性疾病的精准防治提供科学依据与转化方向。
[1] Cohen P, Kajimura S. The cellular and functional complexity of thermogenic fat. Nat Rev Mol Cell Biol. 2021 Jun;22(6):393-409. doi: 10.1038/s41580-021-00350-0IF: 90.2 Q1 .
[2] Morigny P, Boucher J, Arner P, Langin D. Lipid and glucose metabolism in white adipocytes: pathways, dysfunction and therapeutics. Nat Rev Endocrinol. 2021 May;17(5):276-295.
[3] Bayeva M, Sawicki KT, Ardehali H. Taking diabetes to heart--deregulation of myocardial lipid metabolism in diabetic cardiomyopathy. J Am Heart Assoc. 2013 Nov 25;2(6):e000433.
[4] Luo L, Liu M. Adipose tissue in control of metabolism. J Endocrinol. 2016 Dec;231(3):R77-R99.
[5] Martin-Perez M, Urdiroz-Urricelqui U, Bigas C, Benitah SA. The role of lipids in cancer progression and metastasis. Cell Metab. 2022 Nov 1;34(11):1675-1699.
[6] Ouchi N, Parker JL, Lugus JJ, Walsh K. Adipokines in inflammation and metabolic disease. Nat Rev Immunol. 2011 Feb;11(2):85-97.
[7] Roy B, Palaniyandi SS. Tissue-specific role and associated downstream signaling pathways of adiponectin. Cell Biosci. 2021 Apr 26;11(1):77.
[8] Wang W, Seale P. Control of brown and beige fat development. Nat Rev Mol Cell Biol. 2016 Nov;17(11):691-702. doi: 10.1038/nrm.2016.96IF: 90.2 Q1 . Epub 2016 Aug 24.