一、肿瘤免疫逃逸新机制研究取得进展
在肿瘤治疗领域,传统化疗虽可有效杀伤肿瘤细胞,但易诱导耐药性,导致治疗失败;而以PD-1抑制剂为代表的免疫疗法亦面临应答率有限的问题,多数患者因肿瘤免疫逃逸而难以获益。近年来,cGAS-STING通路作为靶向天然免疫的重要方向曾备受关注,但由于该通路在肿瘤组织中激活受限,其临床转化面临瓶颈。
针对上述临床难题,相关研究团队系统揭示了线粒体RNA衍生的危险信号在激活天然免疫及抗肿瘤过程中的关键作用,并明确PNPT1蛋白为该通路的调控核心。基于此,研究提出了一种新的联合治疗策略,为克服肿瘤耐药、提高免疫治疗响应提供了新方向。
该研究成果以“PNPT1-mtRNA axis mediates chemotherapy-induced immune signaling and can be targeted to overcome therapeutic resistance”为题,于2026年1月26日发表于《Vita》。

论文链接:
二、mtRNA:新型免疫警报信号介导广谱抗肿瘤应答
线粒体作为细胞的能量代谢中心,其基因组转录产物mtRNA传统上被认为主要参与能量代谢调控。该研究揭示,mtRNA实际上是一种此前被忽视的关键危险信号,能够突破现有免疫激活通路的局限,诱导更为稳定且广谱的抗肿瘤免疫应答。
研究显示,化疗等抗肿瘤治疗手段可促使肿瘤细胞释放免疫原性双链mtRNA。该信号分子能够特异性激活细胞内的RNA感受器,进而介导下游MAVS信号通路的活化,启动抗肿瘤免疫反应。MAVS通路作为双链RNA诱导免疫应答的核心信号节点,在多种肿瘤组织中均呈现广泛且稳定的表达特征。通过该通路介导的信号转导,mtRNA可高效激活天然免疫,进而促进肿瘤效应性T淋巴细胞的活化与增殖,实现对不同肿瘤类型的广谱免疫激活。
三、PNPT1:肿瘤免疫逃逸与耐药的关键调控因子
尽管mtRNA具有显著的免疫激活作用,肿瘤仍能逃避宿主免疫监视并产生耐药性。通过系统比较肿瘤组织与正常组织的基因表达谱,研究锁定PNPT1蛋白为关键抑制因子。PNPT1是一种3′–5′核酸外切酶,既往研究主要揭示其在线粒体损伤后参与mtRNA降解过程。该研究进一步拓展了对其功能的认知,证实PNPT1在肿瘤组织中呈异常高表达,在肿瘤免疫逃逸与耐药形成中发挥关键调控作用:PNPT1可特异性降解免疫原性双链mtRNA,从源头阻断mtRNA-MAVS免疫通路的激活,抑制天然免疫应答的启动,最终导致肿瘤对化疗及免疫治疗产生耐药。临床数据亦表明,肿瘤组织中PNPT1高表达与患者免疫逃逸、疾病进展及不良预后密切相关。
为验证PNPT1的功能,研究构建了PNPT1敲除模型。结果显示,PNPT1缺失后,双链mtRNA的形成量与释放量显著增加,MAVS通路持续处于激活状态,肿瘤微环境中免疫细胞浸润能力明显增强。该干预策略不仅能诱导强烈的抗肿瘤免疫反应,还可有效逆转实体瘤对化疗和免疫治疗的耐药性,为耐药肿瘤的治疗提供了潜在干预靶点。
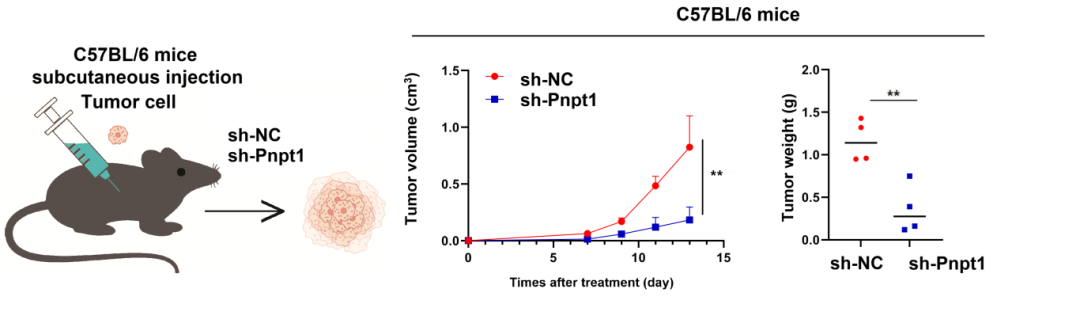 图一:沉默 PNPT1 显著抑制肿瘤生长
图一:沉默 PNPT1 显著抑制肿瘤生长
四、联合治疗策略:协同增效与临床转化前景
基于PNPT1-mtRNA轴的调控机制,研究进一步探索了临床转化路径,提出“PNPT1抑制剂与BH3模拟物联合应用”的治疗策略,展现出良好的临床应用潜力。
BH3模拟物是一类靶向Bcl-2家族蛋白的小分子药物,可有效激活肿瘤细胞线粒体凋亡通路,但目前主要局限于部分血液肿瘤的治疗。研究表明,采用PNPT1抑制剂阻断其降解mtRNA的功能,并与BH3模拟物联合应用,可产生显著的协同抗肿瘤效应。该联合策略中,PNPT1抑制剂解除对mtRNA通路的抑制,高效激活免疫应答;BH3模拟物则通过破坏线粒体膜完整性,进一步促进双链mtRNA的释放,强化免疫激活效果,同时直接诱导肿瘤细胞凋亡,实现“免疫激活与直接杀伤”的双重作用。
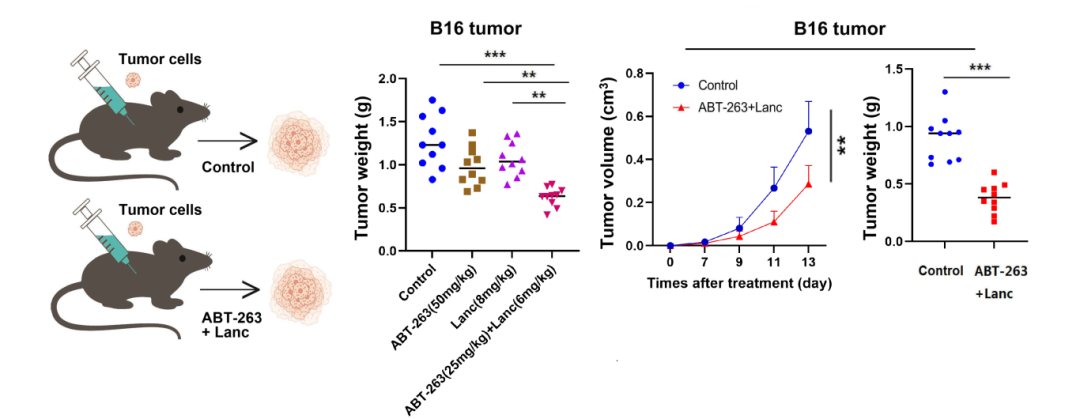 图二:「PNPT1 抑制剂+BH3 模拟物」联合治疗高效抗肿瘤
图二:「PNPT1 抑制剂+BH3 模拟物」联合治疗高效抗肿瘤
值得关注的是,该联合方案在多种小鼠实体瘤模型中表现出高效的抗肿瘤活性,且未观察到明显的全身毒性,为临床转化奠定了重要基础。目前,国际上尚无靶向mtRNA-MAVS通路的疗法报道,该研究填补了这一空白,尤其为STING通路激活受限、对现有治疗耐药的肿瘤提供了新的干预策略。
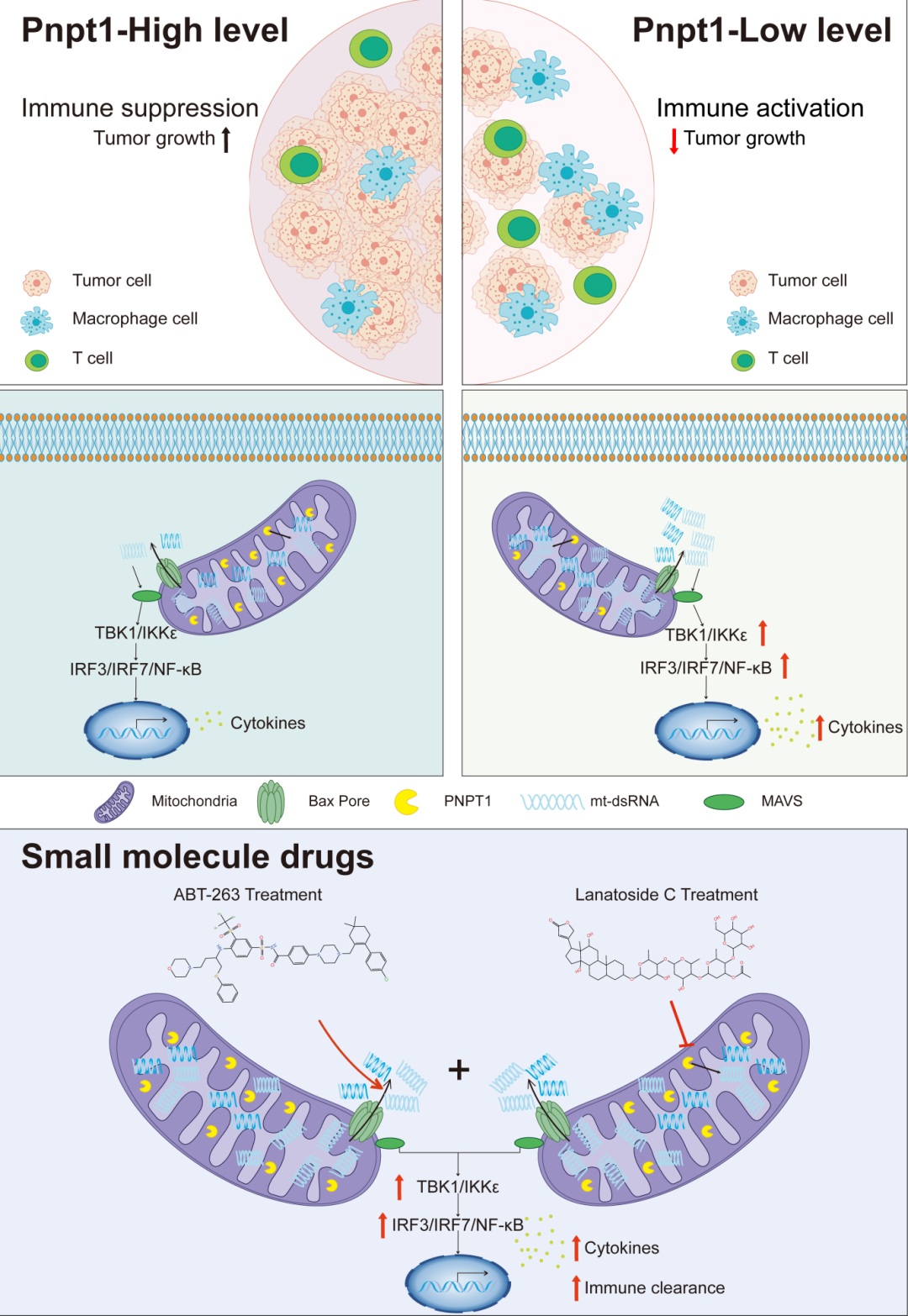
图三: MtRNA-PNPT1 调控肿瘤免疫及联合靶向治疗示意图
综上所述,该研究通过系统解析PNPT1-mtRNA轴的免疫调控机制,突破了肿瘤治疗中耐药、响应率低及单一通路依赖等瓶颈,不仅揭示了mtRNA的新型免疫调控功能,阐明了PNPT1的肿瘤免疫抑制关键作用,还基于机制研究提出了具有转化前景的抗肿瘤新策略,为提升肿瘤免疫治疗效果提供了新的思路。