05. 技术优势
(1)高灵敏度检测能力
可精准识别低丰度蛋白质及其相互作用事件,相较 Western blot、免疫沉淀等传统方法,对微弱信号的捕捉能力显著提升,尤其适用于微量样本或瞬时互作场景的研究。
(2)高特异性识别机制
通过双重特异性抗体匹配与 DNA 连接反应的严格筛选,有效降低非特异性结合导致的假阳性信号。仅当目标蛋白空间距离足够近时,偶联的 DNA 探针才能被连接并启动后续扩增,确保检测结果的可靠性。
(3)原位动态检测特性
支持在细胞或组织样本中进行原位检测,完整保留蛋白质的亚细胞定位与空间分布信息,能真实反映其在生理微环境中的互作状态,避免体外实验导致的人为干扰。
(4)定量分析技术优势
荧光信号的强度与数量和目标蛋白水平呈线性相关,通过标准化数据分析流程,可实现蛋白质相互作用效率与表达量的双重定量,为机制研究提供精准数据支撑。
06. 经典研究案例
案例一:卵巢癌化疗耐药中的信号通路调控研究
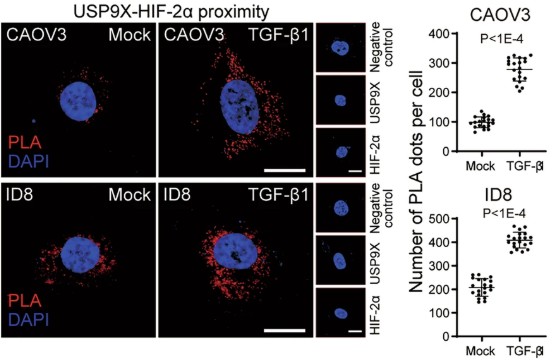
2025 年 4 月,天津医科大学肿瘤医院等机构在相关研究中,运用邻位连接技术(PLA)探索 USP9X 与 HIF-2α、SOX2 蛋白的相互作用机制。研究团队选取 HIF-2α 过表达的 OVCA8 细胞,采用抗 USP9X 与抗 HIF-2α/GAPDH 抗体开展 PLA 实验,在细胞核内观察到显著的 PLA 荧光信号,证实 USP9X 与 HIF-2α 存在直接相互作用,且 TGF-β 刺激与低氧环境可显著增强该互作强度。
此外,通过抗 USP9X 与抗 SOX2 抗体的 PLA 检测发现,USP9X 与 SOX2 在细胞核内呈现共定位特征,尤其在 TGF-β 和低氧处理后,两者的空间邻近信号明显增强。该研究揭示了 USP9X 通过整合 TGF-β 与低氧信号,依赖 HIF-2α 维持肿瘤干细胞特性,进而促进卵巢癌化疗耐药的新机制(Zhang et al., 2025)。
案例二:非小细胞肺癌中的蛋白互作机制研究
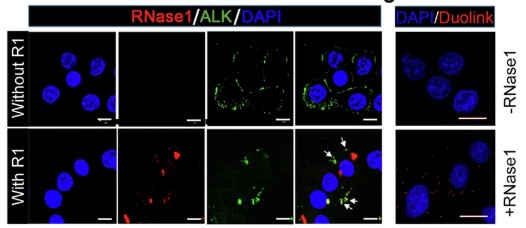
2025 年 4 月,四川大学华西医院刘伦旭团队在相关研究中,借助邻位连接技术(PLA)探究 RNase1、RAGE 与 ALK 蛋白的空间近邻关系。实验通过特异性抗体标记,在细胞水平检测到 RNase1 与 RAGE、RAGE 与 ALK 之间均产生显著 PLA 荧光信号点,证实三种蛋白在细胞内可形成空间邻近的复合体。该发现揭示了 RNase1 驱动 ALK 激活的致癌机制,为非小细胞肺癌的治疗靶点开发提供了新方向(Zha et al., 2025)。